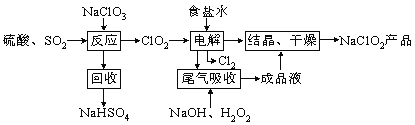
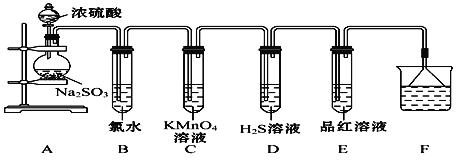
��Ŀ����
����Ŀ��[��ѧһѡ��5���л���ѧ����]
���ںϳ�-���ڵ��ڼ���ҩ���м���Ļ�����H����ϳ�·������ͼ��ͼ��
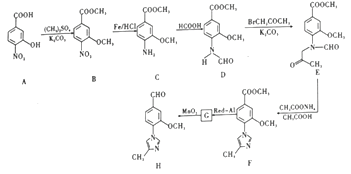
�ش�����������
(1)B�еĺ�������������Ϊ____________��______________ ��___________________��
(2)B��C�ķ�Ӧ����Ϊ_________________��
(3)д��ͬʱ��������������B��һ��ͬ���칹��Ľṹ��ʽ��___________________��
�ٺ��б������ҷ�������һ������̼ԭ�������ܷ���ˮ�ⷴӦ������һ��ˮ����������ֻ��2�ֲ�ͬ��ѧ�������⣬�ҷ����֮��Ϊ2��1��
(4)G�ķ���ʽΪC12H14N2O2���������õ�H��д��G�Ľṹ��ʽ��_____________��
(5)���ݺϳ�·���е���Ϣ����д����![]() ��
��![]() ��(CH3)2SO4Ϊԭ���Ʊ�
��(CH3)2SO4Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ_________________________________(���Լ����ã��ϳ�·������ͼʾ�����������)��
�ĺϳ�·������ͼ_________________________________(���Լ����ã��ϳ�·������ͼʾ�����������)��
���𰸡� �Ѽ� ���� ���� ��ԭ��Ӧ 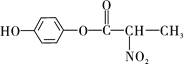
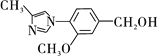
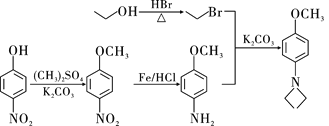
����������1��B�к��������ŵ�����Ϊ�������������Ѽ���
��2��B��C�ķ�Ӧ����Ϊ��ԭ��Ӧ���������ȥ���л�ԭ����
��3��B��ͬ���칹�壬������Ŀ������Ӧ���б�������������Ҫ��ˮ�����֮һֻ�����ֻ�ѧ������ͬ��H��Ϊ2:1���õ��ò���ֻ���ǶԱ����ӡ��������ˮ�����Ϊ�ᣬӦ����3��C��4��O��һ������̼�����������Ͷȡ���������O����һ��̼����Ȼ�������ͱ�������������Ҫ��֤������̼������Ϊ�����������ᡣ�������Ĵ�Ϊ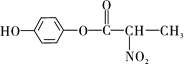 ��д���ɡ�
��д���ɡ�
��4��G�ķ���ʽΪC12H14N2O2���������õ�H��H�ķ���ʽΪC12H12N2O2������G��H�ķ�Ӧ����������ԭ����Ӧ���ǽ����ǻ�����Ϊȩ��������GΪ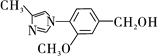 ��
��
��5����(CH3)2SO4��Ŀ�ıȽ�������Ϊ�˽����ǻ���H���ɼ�����B��C�õ�������Fe��HCl��������ԭΪ��������D��E���Եõ���̼�����������������±�����Ͱ�������ȡ�����������ϵ�H�����������������Ϸ������Ϳ��Եõ��ϳɷ�����