题目内容
【题目】将一定质量的镁、铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得的溶液中滴加5mol/L NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如图。
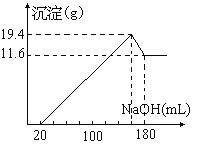
原合金中Mg质量_________,Al质量__________,盐酸的物质的量浓度______________。
【答案】4.8g 2.7g 8 mol/L
【解析】
由图可知,从开始至加入氢氧化钠溶液20mL,没有沉淀产生,说明原溶液中盐酸溶解镁、铝后有剩余,此时发生的反应为盐酸与氢氧化钠的中和反应,继续滴加氢氧化钠溶液,得到最大量沉淀为Mg(OH)2和Al(OH)3,二者质量为19.4g,再继续滴加氢氧化钠溶液,到沉淀不再溶解时,沉淀为Mg(OH)2,质量为11.6g,故Al(OH)3质量为7.8g,由元素守恒可知:n(Al)=n(Al(OH)3)=0.1mol,n(Mg)=n(Mg(OH)2)=0.2mol,m(Al)=2.7g,m(Mg)=4.8g;加入20mL氢氧化钠溶液恰好中和了盐酸,此时溶液的溶质为AlCl3、MgCl2、NaCl,根据钠元素守恒:n(NaCl)=n(NaOH)=0.02L×5mol/L=0.1mol,n(HCl)=3n(AlCl3)+2n(MgCl2)+n(NaCl)=0.8mol,c(HCl)=0.8mol÷0.1L=8 mol/L,故答案为:4.8g;2.7g;8 mol/L。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)水能发生自偶电离2H2O![]() H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程式_______。
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程式_______。
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
化学式 | HNO2 | H2N2O2 |
电离常数 | Ka=5.1×10-4 | Ka1=6.17×10-8、Ka2=2.88×10-12 |
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)_____pH(NaHN2O2)(填“>”、“<”或“=”)。
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=_______(保留三位有效数字)。
③0.lmol/LNa2N2O2溶液中离子浓度由大到小的顺序为____________。
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g)![]() NH2CO2NH4(s) △H1=-159.5kJmol-1;
NH2CO2NH4(s) △H1=-159.5kJmol-1;
反应II:NH2CO2NH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1;
反应III:H2O(l)═H2O(g) △H3=+44.0kJmol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为____________。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为___________。
②图2中能正确反应平衡常数K随温度变化关系的曲线为__________(填字母标号)。

(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为______________。