题目内容
【题目】(题文)50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,完成下列问题: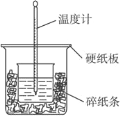
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。请指出装置中的另外错误是 ________________________
(2)烧杯间填满碎纸条的作用是___________。
(3)大烧杯上如不盖硬纸板,求得的中和热值___________(填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50mol·L-1的盐酸跟60 mL 0.55mol·L-1NaOH溶液进行上述实验相比,所放出的热量___________(填“相等”“不相等”),所求中和热___________(填“相等”“不相等”)。
【答案】环形玻璃搅拌棒小烧杯口与大烧杯口不相平减少实验过程中的热量损失偏小不相等相等
【解析】
(1)由量热计的构造可知该装置的缺少的仪器为环形玻璃搅拌棒,中和热测定实验成败的关键是保温,大小烧杯之间应填满碎纸条,作用为保温、隔热,减少实验过程中的热量损失。为了防止热量散失,小烧杯杯口与大烧杯杯口相平。 (2)中和热测定实验关键为保温,大小烧杯之间填满泡沫塑料的作用就是减少实验过程中的热量损失;(3)大烧杯上如果不盖硬纸板,会使一部分热量散失,求得的中和热数值会偏小。 (4)反应放出的热量和所用酸以及碱的量的多少有关,实验中改用60 mL 0.50 mol·L-1的盐酸跟60 mL 0.55 mol·L-1NaOH溶液进行上述实验相比,生成的水的量增多,所放出的热量偏高,但是中和热是指反应生成1mol水时放出的热量,其与酸碱的用量无关,测定的中和热数值相等。

 名校课堂系列答案
名校课堂系列答案