题目内容
氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
传统哈伯法合成氨工艺中相关的反应式为:N2+3H2
2NH3△H<0.
(1)该反应的平衡常数K的表达式为:K=
.降低温度,K值
(2)不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1:3).分析表中数据,
传统哈伯法合成氨工艺中相关的反应式为:N2+3H2
| 催化剂 |
| △ |
(1)该反应的平衡常数K的表达式为:K=
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
增大
增大
(填“增大”“减小”或“不变”).(2)不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1:3).分析表中数据,
200℃、100MPa
200℃、100MPa
(填温度和压强)时H2转化率最高,实际工业生产不选用该条件的主要原因是压强太高,对生产设备要求也高,难以实现
压强太高,对生产设备要求也高,难以实现
.| 压强(MPa) 氨的平衡含量(%) 温度(摄氏度) |
0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
分析:(1)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积;根据温度对平衡移动的影响判断平衡常数的变化;
(2)H2转化率最高时,氨气的含量最大;实际生成时要考虑生成成本、设备能否达到要求等方面.
(2)H2转化率最高时,氨气的含量最大;实际生成时要考虑生成成本、设备能否达到要求等方面.
解答:解:(1)根据化学方程式可写出平衡常数为k=
,由于反应放热,降低温度平衡向正反应方向移动,则平衡常数增大,
故答案为:
;增大;
(2)200℃、100MPa时氨气的含量最大,则H2转化率最高,但实际工业生产中越强不能太大,因压强太高,对生产设备要求也高,难以实现,
故答案为:200℃、100MPa;压强太高,对生产设备要求也高,难以实现.
| c2(NH3) |
| c(N2)?c3(H2) |
故答案为:
| c2(NH3) |
| c(N2)?c3(H2) |
(2)200℃、100MPa时氨气的含量最大,则H2转化率最高,但实际工业生产中越强不能太大,因压强太高,对生产设备要求也高,难以实现,
故答案为:200℃、100MPa;压强太高,对生产设备要求也高,难以实现.
点评:本题考查了化学平衡常数及合成氨条件选择,可以根据所学知识完成,注意工业生产中必须考虑生成成本、经济效益,本题难度不大.

练习册系列答案
相关题目
氨是一种重要的化工原料,氨的合成与应用是当今重要研究内容之一。不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2起始物质的量之比为1∶3)。
|
衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
回答下列有关问题:
(1)利用表中数据推断得出合成氨的反应是__________反应(填“放热”、“吸热”或“无热量变化”)。
(2)根据表中数据,在200℃和100MPa时,平衡体系中NH3的物质的量分数最高,而实际工业生产不选用该条件的主要原因是___________________________________。
(3)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“可能增大也可能减小”):
| 反应速率 | 平衡常数K | 氨的体积分数 | |
| 变化情况 |
(4)将1molH2和1molN2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,测得NH3的物质的量为0.3mol,此时若移走0.5molH2和0.5molN2,则反应达到新的平衡时,NH3的物质的量为_____________(选填答案编号)。
A.0.3mol B.0.15mol C.小于0.15mol D.大于0.15mol,小于0.3mol
 ;
; 压强(Mpa)
压强(Mpa) 氨的平
氨的平 2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。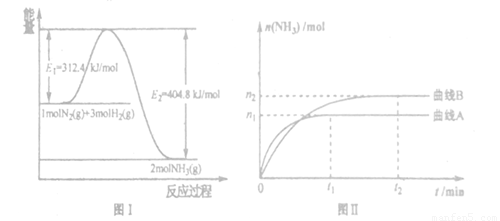
 mol/(L·min)
mol/(L·min) 倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______
倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______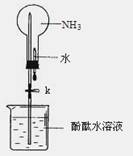

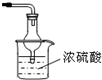
 Cu + Cu2+)。
Cu + Cu2+)。