题目内容
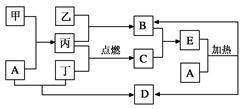
(12分)已知金属单质A是生产生活中用量最大的金属。 D是难溶于水的白色固体。 F为红褐色固体。无色气体甲遇气体丙立即生成红棕色的气体乙。(图中部分产物和反应的条件略)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式C__________G__________。
写出反应①的化学方程式________________________________ 。
反应②的离子方程式_____________________________。
(3)反应④整个过程观察到的现象为_____________________________。
(4)反应⑤中,若将充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积_______________。
(5)某种贫血症患者应补充C物质的阳离子。含该离子的药片外表包有一层特殊的糖衣,这层糖衣的作用就是保护该离子不被空气中的氧气氧化。为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴__________溶液,溶液显__________色,表明该药片已失效。
(1)Fe(NO3)2、Na2O2;(2)4HNO3+Fe=Fe(NO3)3+NO↑+2H2O;Fe + 2Fe3+ = 3Fe2+;
(3)白色沉淀迅速变为灰绿色,最后变为红褐色;(4)2/3;(5)硫氰酸钾 红
解析试题分析:根据题意知,金属单质A是生产生活中用量最大的金属,则A为铁;F为红褐色固体,则F为氢氧化铁;无色气体甲遇气体丙立即生成红棕色的气体乙,则甲为一氧化氮,丙为氧气,乙为二氧化氮;结合题给转化关系图及相关物质的性质知,B为硝酸铁,C为硝酸亚铁,D为氢氧化亚铁,E为硝酸,H为氢氧化钠,G为过氧化钠。(1)根据上述分析知,C为硝酸亚铁,G为过氧化钠,化学式分别为Fe(NO3)2、Na2O2;(2)反应①为铁与稀硝酸反应生成硝酸铁、一氧化氮和水,化学方程式为4HNO3+Fe=Fe(NO3)3+NO↑+2H2O;反应②为硝酸铁与铁反应生成硝酸亚铁,离子方程式为Fe + 2Fe3+ = 3Fe2+;(3)反应④为氢氧化亚铁被空气中的氧气氧化为氢氧化铁,整个过程观察到的现象为白色沉淀迅速变为灰绿色,最后变为红褐色;(4)反应⑤为二氧化氮与水反应生成硝酸和一氧化氮,根据化学方程式3NO2+H2O=2HNO3+NO判断,充分反应后,试管内液体占试管总体积的2/3;(5)根据题意知,贫血症患者应补充C物质的阳离子为亚铁离子,被空气中的氧气氧化转化为铁离子,为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴硫氰酸钾溶液,溶液显红色,表明该药片已失效。
考点:本题为无机框图题,考查铁、钠等单质及其化合物的性质和相互转化关系。

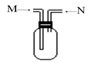
已知下列转化关系中M、N均为单质,则M可能是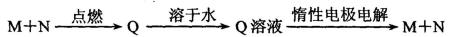
| A.Na | B.Fe | C.O2 | D.H2 |

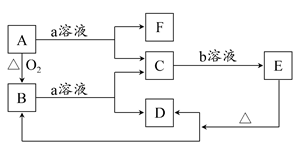
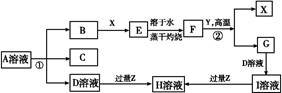
 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题: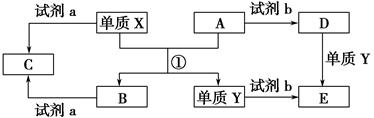

 (1)写出常温下单质X2与Z反应的离子方程式
(1)写出常温下单质X2与Z反应的离子方程式