题目内容
下列说法正确的是
| A.已知:2H2(g)+O2(g)=2H2O(l)△H<0,反应物总能量小于生成物总能量 |
| B.测定盐酸和氢氧化钠反应的中和热实验中,所用试剂可以是浓溶液 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ |
| D.已知C(s)与CO(g)的燃烧热分别为393.5kJ·mol-1 、283.0kJ·mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol |
D
正确答案D
A.由反应:2H2(g)+O2(g)=2H2O(l) △H<0,是放热反应,反应物总能量高于生成物总能量。
B.测定盐酸和氢氧化钠反应的中和热实验中,所用试剂不可以是浓溶液,浓溶液稀释时也有热效应。
C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量大于114.6kJ ,Ba2+与SO42―结合生成BaSO4时也要放热。
D.已知C(s)与CO(g)的燃烧热分别为393.5kJ·mol-1 、283.0kJ·mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol
C(s)+O2(g)=CO2(g) △H1=―393.5kJ·mol-1
CO(g)+1/2O2(g)=CO2(g) △H2=―283.0kJ·mol-1
由盖斯定律得C(s)+1/2O2(g)="CO(g)" △H=△H1―△H2=-110.5kJ/mol

练习册系列答案
相关题目
 __7(填>,<或=),原因是 _______________________________________________________________________________
__7(填>,<或=),原因是 _______________________________________________________________________________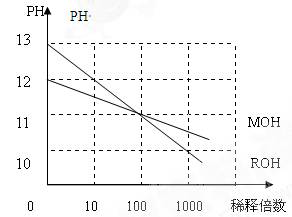
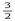 O2(g)===CO2(g)+2H2O(l);ΔH="+725.8" kJ/mol
O2(g)===CO2(g)+2H2O(l);ΔH="+725.8" kJ/mol