题目内容
海水中含有丰富的镁资源。工业上常用海水晒盐后的苦卤水提取Mg,流程如下图所示:

(1)工业制取镁的方法是 法。
(2)试剂Ⅰ一般选用 (填化学式)。
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。

①由图可知Mg与卤素单质的反应均为 (填“放热”或“吸热”)反应;推测化合物的热稳定性顺序为MgI2 MgF2(填“>”、“=”或“<”)。
②依上图数据写出MgBr2(s)与Cl2(g)反应的热化学方程式 。
(4)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体生成。写出CH3MgCl水解的化学方程式 。
(5)向Mg(OH)2中加入NH4Cl溶液,可使沉淀溶解,请结合平衡原理和必要的文字解释原因 。
(1)电解法或电解熔融氯化镁
(2)Ca(OH)2(该空1分) (3)①放热(该空1分),<
②MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l) △H=-117KJ·mol—1
(4)CH3MgCl+H2O=CH4↑+Mg(OH)Cl↓或2CH3MgCl+2H2O=2CH4↑+Mg(OH)2↓+MgCl2
(5)Mg(OH)2(s)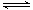 Mg2+(aq)+2OH¯(aq),向Mg(OH)2中加入NH4Cl溶液后,铵根离子结合氢氧根离子生成一水合氨,降低了氢氧根离子浓度,使氢氧化镁沉淀的溶解平衡向右移动,从而沉淀溶解。
Mg2+(aq)+2OH¯(aq),向Mg(OH)2中加入NH4Cl溶液后,铵根离子结合氢氧根离子生成一水合氨,降低了氢氧根离子浓度,使氢氧化镁沉淀的溶解平衡向右移动,从而沉淀溶解。
【解析】
试题分析:(1)镁是活泼的金属,工业制取镁的方法是电解熔融的氧化镁,即电解法冶炼镁。
(2)要将溶液中的Mg2+转化为氢氧化镁沉淀,需要加入碱。考虑试剂的来源和经济效益,一般加入的是氢氧化钙,化学式为Ca(OH)2。
(3)①由图可知反应物的总能量均高于生成物的总能量,所以Mg与卤素单质的反应均为放热反应。镁与单质氟反应放出的热量最多,则生成的MgF2稳定性最强,所以化合物的热稳定性顺序为MgI2 <MgF2。
②根据图像可知,Mg(s)+Cl2(g)=MgCl2(s) △H=-641kJ/mol、Mg(s)+Br2(l)=MgBr2(s) △H=-524kJ/mol,则根据盖斯定律可知,前者减去后者即得到反应MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l),所以该反应的反应热△H=-641kJ/mol+524kJ/mol=-117KJ/mol。
(4)CH3MgCl易与水发生水解反应并有无色无味气体生成,则该气体应该是甲烷。所以根据原子守恒可知,另外的生成物是碱式氯化镁,因此CH3MgCl水解的化学方程式为CH3MgCl+H2O=CH4↑+Mg(OH)Cl↓或2CH3MgCl+2H2O=2CH4↑+Mg(OH)2↓+MgCl2。
(5)氢氧化镁溶于水存在溶解平衡Mg(OH)2(s)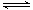 Mg2+(aq)+2OH¯(aq),铵根离子结合氢氧根离子生成一水合氨,降低了氢氧根离子浓度,使氢氧化镁沉淀的溶解平衡向右移动,沉淀溶解。
Mg2+(aq)+2OH¯(aq),铵根离子结合氢氧根离子生成一水合氨,降低了氢氧根离子浓度,使氢氧化镁沉淀的溶解平衡向右移动,沉淀溶解。
考点:考查金属镁的冶炼、试剂的性选择、物质稳定性判断、热化学方程式的书写、水解应用以及外界条件对溶解平衡的影响

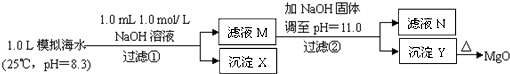
(2011?浙江)海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案:
|
海水中含有丰富的镁资源.某同学设计了从模拟海水中制备Mg0的实验方案( )
已知:Kap[Mg(OH)4]=5.61×10-12 下列说法正确的是( ) |