题目内容
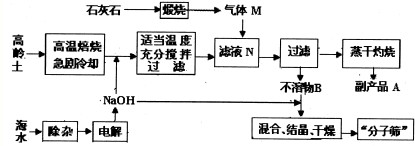
(2011?浙江)海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案:
|
分析:步骤①,加入0.001mol NaOH时,OH- 恰好与HCO3-完全反应,生成0.001molCO32-.由于Ksp(CaCO3)<<Ksp(MgCO3),生成的CO32-与水中的Ca2+反应生成CaCO3 沉淀,滤液M中同时存在着Ca2+和Mg2+;
步骤②,当滤液M中加入NaOH 固体,调至pH=11(即pOH=3)时,此时滤液中c(OH-)=1×10-3 mol?L-1.
根据溶度积可判断无Ca(OH)2生成,有Mg(OH)2沉淀生成.
步骤②,当滤液M中加入NaOH 固体,调至pH=11(即pOH=3)时,此时滤液中c(OH-)=1×10-3 mol?L-1.
根据溶度积可判断无Ca(OH)2生成,有Mg(OH)2沉淀生成.
解答:解:A.步骤①,从题给的条件,可知n(NaOH )=0.001mol,[即n(OH-)=0.001mol].依据离子反应“先中和、后沉淀、再其他”的反应规律,当1L模拟海水中,加入0.001mol NaOH时,OH- 恰好与HCO3-完全反应:OH-+HCO3-=CO32-+H2O,生成0.001molCO32-.由于Ksp(CaCO3)<<Ksp(MgCO3),生成的CO32-与水中的Ca2+反应生成CaCO3 沉淀Ca2++CO32-=CaCO3↓.所以沉淀物X为CaCO3,故A正确;
B.由于CO32-只有0.001mol,反应生成CaCO3 所消耗的Ca2+也只有0.001mol,滤液中还剩余c(Ca2+)=0.010 mol?L-1.滤液M中同时存在着Ca2+和Mg2+,故B错误;
C.步骤②,当滤液M中加入NaOH 固体,调至pH=11(即pOH=3)时,此时滤液中c(OH-)=1×10-3 mol?L-1.则
Q[Ca(OH)2]=c(Ca2+)×(10-3)2=0.010×(10-3)2=10-8<Ksp[Ca(OH)2],无Ca(OH)2生成.
Q[Mg(OH)2]=c(Mg2+)×(10-3)2=0.050×(10-3)2=5×10-8>Ksp[Mg(OH)2],有Mg(OH)2沉淀生成.
又由于Ksp[Mg(OH)2]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6<10-5,无剩余,滤液N中不存在Mg2+,
故C错误;
D.步骤②中若改为加入4.2 g NaOH固体,则n(NaOH)=0.105mol,与0.05mol Mg2+反应:Mg2++2OH-=Mg(OH)2↓,生成0.05 mol Mg(OH)2,剩余0.005 mol OH-.
由于Q[Ca(OH)2]=c(Ca2+)×(OH-)2=0.010×(0.005)2=2.5×10-7<Ksp[Ca(OH)2],所以无Ca(OH)2沉淀析出,沉淀物Y为Mg(OH)2沉淀,故D错误.
故选A.
B.由于CO32-只有0.001mol,反应生成CaCO3 所消耗的Ca2+也只有0.001mol,滤液中还剩余c(Ca2+)=0.010 mol?L-1.滤液M中同时存在着Ca2+和Mg2+,故B错误;
C.步骤②,当滤液M中加入NaOH 固体,调至pH=11(即pOH=3)时,此时滤液中c(OH-)=1×10-3 mol?L-1.则
Q[Ca(OH)2]=c(Ca2+)×(10-3)2=0.010×(10-3)2=10-8<Ksp[Ca(OH)2],无Ca(OH)2生成.
Q[Mg(OH)2]=c(Mg2+)×(10-3)2=0.050×(10-3)2=5×10-8>Ksp[Mg(OH)2],有Mg(OH)2沉淀生成.
又由于Ksp[Mg(OH)2]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6<10-5,无剩余,滤液N中不存在Mg2+,
故C错误;
D.步骤②中若改为加入4.2 g NaOH固体,则n(NaOH)=0.105mol,与0.05mol Mg2+反应:Mg2++2OH-=Mg(OH)2↓,生成0.05 mol Mg(OH)2,剩余0.005 mol OH-.
由于Q[Ca(OH)2]=c(Ca2+)×(OH-)2=0.010×(0.005)2=2.5×10-7<Ksp[Ca(OH)2],所以无Ca(OH)2沉淀析出,沉淀物Y为Mg(OH)2沉淀,故D错误.
故选A.
点评:这是一道新颖的计算型分析推断题,命题者通过精心选择,以从模拟海水中制备MgO的实验方案为背景,结合考查有关溶度积的概念及计算,把一个具体情景与教材的知识内容有机结合起来.要求考生定量地分析发生的反应,溶液中存在的离子,推断沉淀是否产生,从而得出正确的结论.计算强调了实用性以及认识、解决问题的综合性,体现了新课程的特色.

练习册系列答案
相关题目
 (2011?浙江)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )
(2011?浙江)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( ) KI3
KI3

 →碘单质.下列叙述正确的是( )
→碘单质.下列叙述正确的是( )