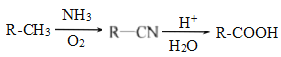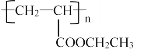题目内容
【题目】有机物 A 是未成熟葡萄中含有的一种物质,由 C、H、O 三种元素组成,A 在气态时的密度是相同条件下氢气密度的 38 倍。在一定条件下 A 既可以与乙醇反应生成酯又可以与乙酸反应生成酯。已知 0.1mol A 完全燃烧时生成 0.2mol CO2 和 0.2mol H2O;1mol A 可与 2mol Na 或 1mol NaOH 反应。试确定:
(1)有机物 A 的分子式_________________;
(2)写出在浓硫酸作用下,两分子 A 相互反应生成六元环状物质的化学方程式______________。
【答案】C2H4O3 
【解析】
根据密度与相对分子质量成正比,求出相对分子质量,再根据生成的CO2 和 H2O的物质的量,求出碳原子和氢原子的个数,最后求出氧原子的个数,得到分子式;根据与 Na 或 NaOH 反应,得到含有的官能团和官能团的个数,得到结构式,由此解题。
(1) 根据相同条件下,气体的密度比等于相对分子质量之比,得A的相对分子质量是38×2 =76,由0.1mol A 完全燃烧时生成0.2mol CO2和0.2mol H2O得每个分子中含有2个碳原子和4个氢原子,设A 的分子式为C2H4Ox,则2×12+4×1+x×16=76,得x=3,分子式为C2H4O3;
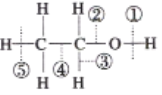
(2) 由1mol A 可与 2mol Na 或 1mol NaOH 反应,可知分子中含有一个羟基和一个羧基,则A结构为 ,在浓硫酸作用下,两分子A 相互间发生酯化反应形成六元环状物质,化学方程式为
,在浓硫酸作用下,两分子A 相互间发生酯化反应形成六元环状物质,化学方程式为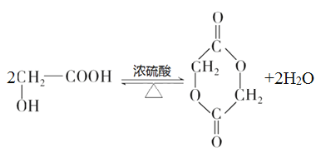 。
。

 阅读快车系列答案
阅读快车系列答案【题目】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2 L的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法正确的是( )
A. 当容器中气体的密度不变时,该反应达到平衡状态
B. 该反应进行到第3分钟时,逆反应速率小于正反应速率
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L·min)
D. 容器内达到平衡状态时的压强与起始时的压强之比为5∶4