题目内容
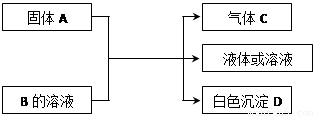
(⑸题3分,其余每空2分,共15分)四种短周期元素A、D、E、G,原子序数依次增大,A、G同主族,D、E同周期;A和D、E、G的单质都可以在一定条件下化合依次生成共价化合物甲、乙和离子化合物丙,丙和乙剧烈反应得到强碱溶液X和A的单质。请回答:
⑴化合物丙和乙的反应的化学方程式是________________ ;
⑵A和E两种元素构成的一种化合物,其水溶液显弱酸性,试用恰当的方程式解释该溶液呈弱酸性的原因_____________________________________________________ ;
⑶将A、D、E三种元素构成的一种化合物与X恰好反应,所得溶液呈碱性;试用恰当的方程式解释该溶液呈碱性的原因__________________________________________,该溶液中存在的离子有(请用离子符号按浓度由大到小的顺序以“>”连接填写)__________________________________________ ;
⑷在丙和乙的反应中,当转移1.5mol电子时,得到A单质__________ g;若同时得到X的溶液0.50L,则所得溶液的物质的量浓度为__________________________。
⑸工业制取甲的反应为:D2(g)+3A2(g) 2甲(g) ;△H<0 。若改变下列任何一个条件(其它条件不变)时,上述平衡一定向右移动的是(填写序号)_________________ (3分) 。
2甲(g) ;△H<0 。若改变下列任何一个条件(其它条件不变)时,上述平衡一定向右移动的是(填写序号)_________________ (3分) 。
A.将甲不断从反应体系中分离 B.减小反应体系的压强 C.降低反应体系的温度
D.加入适当的催化剂 E.向体系中充入D2和A2
(⑸题3分,其余每空2分,共15分)
⑴ NaH+H2O=NaOH+H2↑;
⑵H2O2 H++HO2-
;
H++HO2-
;
⑶ NO2-+H2O HNO2+OH-,
Na+>NO2->OH->H+ ;
HNO2+OH-,
Na+>NO2->OH->H+ ;
⑷ 3.0; 3.0 mol·L-1 ; ⑸ A.C.E (3分)
【解析】根据元素的结构、位置及性质可知,A、D、E、G分别是H、N、O、Na。
(1)丙是氢化钠,乙是水,方程式为NaH+H2O=NaOH+H2↑。
(2)氢和氧形成的双氧水,能电离出氢离子,显酸性,方程式为H2O2 H++HO2-
。
H++HO2-
。
(3)和氢氧化钠反应的生成物显碱性,说明应该是弱酸,所以生成物是亚硝酸钠,水解方程式为NO2-+H2O HNO2+OH-。其离子浓度大小顺序为Na+>NO2->OH->H+。
HNO2+OH-。其离子浓度大小顺序为Na+>NO2->OH->H+。
(4)根据方程式NaH+H2O=NaOH+H2↑可知,每生成1mol氢气,转移电子是1mol,所以当转移1.5mol电子时,得到氢气是1.5mol,质量是3.0g。生成的氢氧化钠是1.5mol,所以其浓度是1.5mol÷0.5L=3.0mol/L。
(6)该反应是氨气的合成,A是降低氨气的浓度,平衡向正反应方向移动。正反应是体积减小的,所以降低压强,平衡向逆反应方向移动。正反应放热,所以降低温度,平衡向正反应方向移动。催化剂不能改变平衡状态,D不正确。增大反应物的浓度,平衡向正反应方向移动。答案选ACE。


 2甲(g) ;△H<0 。若改变下列任何一个条件(其它条件不变)时,上述平衡一定向右移动的是(填写序号)_________________ (3分) 。
2甲(g) ;△H<0 。若改变下列任何一个条件(其它条件不变)时,上述平衡一定向右移动的是(填写序号)_________________ (3分) 。