题目内容
18.下列反应的离子方程式书写正确的是( )| A. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O |
分析 A.氨水为弱碱,二者反应生成氢氧化铝沉淀;
B.醋酸为弱酸,离子方程式中醋酸不能拆开;
C.离子方程式两边总电荷不相等,违反了电荷守恒;
D.澄清石灰水中的氢氧化钙应该拆开.
解答 解:A.氯化铝溶液中加入过量氨水的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A正确;
B.醋酸和碳酸钙都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.氯化亚铁溶液中通入氯气生成氯化铁,正确的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.澄清石灰水与稀盐酸的反应实质为氢离子与氢氧根离子反应生成水,正确的离子方程式为:OH-+H+═H2O,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
9.50g质量分数为19%的氧化镁溶液中Cl-的物质的量为( )
| A. | 0.01mol | B. | 0.1mol | C. | 0.02mol | D. | 0.2mol |
6.下列说法中正确的是( )
| A. | 烧菜用过的铁锅,经放置因发生氧化还原反应常出现红棕色斑迹 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量的MgSO4 | |
| C. | 蒸馏时温度计时用来测定蒸馏烧瓶中液体的温度 | |
| D. | 用加热、蒸发的方法可以除去NaCl中CaCl2、MgCl2等杂质 |
3.下列叙述中,正确的是( )
| A. | 硫酸的摩尔质量是98g | B. | 1mol N2的质量为28g/mol | ||
| C. | 摩尔是物质的量的单位 | D. | 1mol氧的质量等于16g |
7.下列叙述中错误的是( )
| A. | H2SO4的摩尔质量是98 g•mol-1 | |
| B. | 2mol NO和2mol N2气体体积相等 | |
| C. | 等质量的O2和O3中所含氧原子个数相同 | |
| D. | 等物质的量的CO和CO2中所含碳原子数相等 |
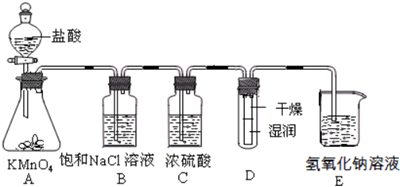
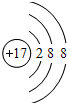 .
.