题目内容
中和滴定是利用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸),
若用A代表酸,用B代表碱,可以利用下式来计算未知碱的物质的量浓度的是(ν为化学计量数)
A.cB=![]() B.cB=
B.cB=![]() C.cB=
C.cB=![]() D.cB=
D.cB=![]()
A
解析:
中和反应νA A---------- -----------νBB,
νA νB
CA·VA CB·VB
νA : νB =CA·VA : CB·VB
cB=![]()

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2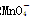 +
+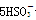 +H+===2Mn2++5
+H+===2Mn2++5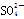 +3H2O,填空回答问题:
+3H2O,填空回答问题:
(1)该滴定实验所需仪器有下列中的________(填序号)。
| A.酸式滴定管(50 mL) | B.碱式滴定管(50 mL) |
| C.量筒(10 mL) | D.锥形瓶 |
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:
________________________________________________________________________。
(3)选何种指示剂,说明理由
________________________________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积偏________(填“多”或“少”)。根据(b-a) mL计算得到的待测浓度,比实际浓度偏________(填“大”或“小”)。
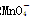 +
+ +H+===2Mn2++5
+H+===2Mn2++5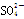 +3H2O,填空回答问题:
+3H2O,填空回答问题:


