题目内容
工业上制CuCl2时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉(含杂质FeO)充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.
(1)在除去溶液中Fe2+时,可采用的方法是
[ ]
A.直接加碱,调整溶液pH=9.6
B.加纯铜,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3~4
D.通入H2S,使Fe2+直接沉淀
(2)工业上除去溶液中Fe2+,常使用NaClO,向溶液中加NaClO后,溶液的pH的变化是
[ ]
A.肯定减小
B.肯定增大
C.可能减小
D.可能增大
答案:C;D

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
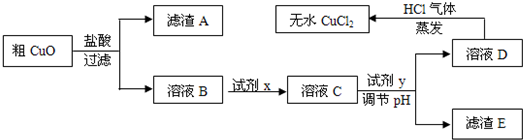
 已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
 mol
mol ×100℅
×100℅