题目内容
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:![]()
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
A. 溶液颜色保持不变,说明上述可逆反应达到平衡状态
B. 若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g
C. 常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6
D. 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
【答案】B
【解析】试题分析: CrO42﹣为黄色的,Cr2O72﹣为橙色的,溶液颜色保持不变,说明各物质的浓度不再改变,则反应达到达平衡状态,A对,不选;液中铬元素的含量为28.6 g/L,在1L废水中铬元素的物质的量为n(Cr)="28.6g/L×1l÷" 52g/mol ="0.55mol" , Cr的化合价为 +6价,反应后变为+3价,Fe2+反应后变为Fe3+,根据氧化还原反应中电子得失数目相等可得:n(Fe2+)=3×0.55mol=1.65mol,则m(FeSO4·7H2O) = 1.65mol×278g/mol=458.7g,B错,选B;反应 2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O的平衡常数为K= c(Cr2O72-)/ c2(H+)·c(CrO42-),c(CrO42-)=[(28.6÷52)÷11]mol/L=0.05mol/L,c(Cr2O72-)=(11÷2)×c(CrO42-)=0.25mol/L,则可得c(H+)=10-6mol/L,故pH=6,C对,不选;根据溶度积的表达式有: c(Cr3+)·c3(OH-)=1×10﹣32,c3(OH-)=10﹣32÷10﹣5=10﹣27,得c(OH-)=1×10﹣9,则c(H+)=10﹣5,所以 pH=5,D对,不选。
Cr2O72﹣(aq)+H2O的平衡常数为K= c(Cr2O72-)/ c2(H+)·c(CrO42-),c(CrO42-)=[(28.6÷52)÷11]mol/L=0.05mol/L,c(Cr2O72-)=(11÷2)×c(CrO42-)=0.25mol/L,则可得c(H+)=10-6mol/L,故pH=6,C对,不选;根据溶度积的表达式有: c(Cr3+)·c3(OH-)=1×10﹣32,c3(OH-)=10﹣32÷10﹣5=10﹣27,得c(OH-)=1×10﹣9,则c(H+)=10﹣5,所以 pH=5,D对,不选。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 氢气 | 加热 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
A.A
B.B
C.C
D.D
【题目】下列说法正确的是
A. 铵盐不稳定,受热分解都产生氨气
B. 向硅酸钠液中加适量稀盐酸,有透明的凝胶形成
C. 由于浓硫酸有强氧化性,因此不能用铁罐存浓硫酸
D. 浓硝酸不稳定,实验保存在无色试剂瓶中
【题目】如下图所示的实验装置用于研究温度对凝乳酶催化乳汁凝固的影响。
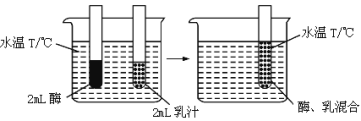
先将酶和乳汁分别装入2支试管中,再将2支试管放入同一水浴(温度用℃表示)环境中持续15min,最后将酶和乳汁倒入同一试管中混合,保温并记录凝乳所需要的时间。多次实验并记录在不同温度下所需要的时间,其结果记于下表:
装置 | A | B | C | D | E | F |
水浴温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 |
凝乳时间(min) | 很长 | 7.0 | 4.0 | 1.5 | 4.0 | 不凝乳 |
(1)解释以下两种处理对实验结果的影响。
①将装置A中的混合物加温至40℃,乳汁凝固时间如何变化? (明显缩短/明显增加/时间不变/不会凝固)
②装置F中的混合物冷却至40℃, 乳汁凝固时间如何变化? (明显缩短/明显增加/时间不变/不会凝固)。原因是 。
(2)若将酶和乳汁先混合再进行F组实验,实验结果会不准确,原因是什么 。
(3)为进一步探究该酶催化作用的最适温度,应在 范围内设置更小的温度梯度,其他条件不变,重新进行实验,凝乳时间最短对应的温度接近最适温度。