题目内容
(5分)在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)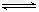 pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值① ,混合气体的密度② ;降温时,混合气体的平均相对分子质量 ③ ;加入催化剂,气体的总物质的量④ ;充入C,则A、B的物质的量⑤。(增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值① ,混合气体的密度② ;降温时,混合气体的平均相对分子质量 ③ ;加入催化剂,气体的总物质的量④ ;充入C,则A、B的物质的量⑤。(增大、减小、不变、不确定)
①减小 ②不变 ③减小 ④不变 ⑤增大(各1分共5分)
解析试题分析:在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)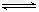 pC(g)处于平衡状态(已知n+m>p,△H>0),反应放热,所以升高温度,平衡向正向移动,反应物减少,生成物增加,c(B)/c(C)的比值减少, 气体混合气体的密度p=m/v,反应前后,气体质量守恒,体积又不变,所以气体混合气体的密度。降温时平衡向逆向移动反应物增加,生成物减少,气体的平均相对分子质量=m气体总/n气体总 而且n+m>p 气体质量守恒,气体总物质的量增大,所以混合气体的平均相对分子质量减小。加入催化剂,平衡不移动,气体的总物质的量不变。
pC(g)处于平衡状态(已知n+m>p,△H>0),反应放热,所以升高温度,平衡向正向移动,反应物减少,生成物增加,c(B)/c(C)的比值减少, 气体混合气体的密度p=m/v,反应前后,气体质量守恒,体积又不变,所以气体混合气体的密度。降温时平衡向逆向移动反应物增加,生成物减少,气体的平均相对分子质量=m气体总/n气体总 而且n+m>p 气体质量守恒,气体总物质的量增大,所以混合气体的平均相对分子质量减小。加入催化剂,平衡不移动,气体的总物质的量不变。
充入C 平衡向逆向移动 则 A、B的物质的量增大
考点:化学平衡的影响因素
点评:本题考查的是温度变化对化学平衡的影响,对反应前后体积变化的反应,气体的平均相对分子质量随气体总质量和气体总的物质的量变化而变化。浓度,温度,压强(针对气体) PV="nRT" 其中P代表压强,V 代表体积,n物质的量浓度 R 表示常数T 表示温度。 在液体反应中,反应物浓度越高其正反应速率越大。一种反应物浓度越大,其自身转化率越低,其他的反应物转化率越高。在气体反应中,恒温恒容时,充入反应物气体,也相当于加大其浓度,结果同上。 如果正反应是吸热,加热可以促进正反应(其实正逆反应都要促进,只是正反应促进的程度大),降温促进逆反应。 在恒温密闭容器中,反应两边化学计量数不等时,加压,平衡朝着化学计量数小的那一方移动,加压相当于增加了反应物的浓度。 当然这些得根据列夏特勒原理来判断。

