题目内容
14.下列电离方程式,不正确的是( )| A. | NaOH═Na++OH- | B. | H2SO4═H2++SO42- | C. | KClO3═ClO3-+K+ | D. | NaCl═Na++Cl- |
分析 A.氢氧化钠为强电解质,完全电离,用等号;
B.硫酸为强电解质,完全电离,氢离子符合表示错误;
C.氯酸钾为强电解质,完全电离生成钾离子和氯酸根离子;
D.氯化钠为强电解质,完全电离生成钠离子与氯离子.
解答 解;A.氢氧化钠为强电解质,完全电离,电离方程式:NaOH═Na++OH-,故A正确;
B.硫酸为强电解质,完全电离,电离方程式:H2SO4═2H++SO42-,故B错误;
C.氯酸钾为强电解质,完全电离,电离方程式:KClO3═ClO3-+K+,故C正确;
D.氯化钠为强电解质,完全电离,电离方程式:NaCl═Na++Cl-,故D正确;
故选:B.
点评 本题考查了电离方程式书写,明确电解质强弱,书写电离方程式方法是解题关键,注意离子的正确书写、电荷守恒、离子团不能拆开,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
4.下列有机物命名正确的是( )
| A. | 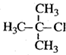 2-甲基-2-氯丙烷 | B. | 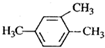 1,3,4-三甲苯 | C. | 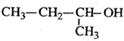 2-甲基-1-丙醇 | D. | 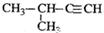 2-甲基-3-丁炔 |
5.铁和铁合金是生活中常用的材料,下列说法正确的是( )
| A. | 不锈钢是铁合金,只含金属元素 | |
| B. | 生铁的含碳量比钢高 | |
| C. | 铁与盐酸反应,铁合金不与盐酸反应 | |
| D. | 铁合金的熔点低于纯铁的熔点 |
2.下列说法正确的是( )
| A. | 电池充电时其正极应与外电源的负极相连而成为阴极 | |
| B. | 氢氧燃料电池(碱性介质)的正极反应式:O2+4e-→2O2- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜 | |
| D. | 铁件上镀铜时,将铁件与电源的负极相连 |
19.下列物质中分子数最多的是( )
| A. | 标准状况下134.4LNH3 | B. | 132g CO2 | ||
| C. | 标准状况下108 mL 水 | D. | 6.02×1024个氢分子 |
6.实验室需用90mL0.1mol/L的硫酸铜溶液,用100mL的容量瓶配制,以下配制操作正确的是( )
| A. | 称取1.44g硫酸铜,配成100mL溶液 | B. | 称取2.25g胆矾,加入100mL水 | ||
| C. | 称取1.6g硫酸,加入100mL水 | D. | 称取2.5g胆矾,配成100mL溶液 |
3.标准状况下,现有①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是( )
| A. | 体积:②>③>①>④ | B. | 物质的量:②>③>④>① | ||
| C. | 质量:②>③>①>④ | D. | 氢原子个数:①>③>④>② |