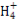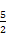题目内容
用下列实验装置进行相应实验,能达到实验目的的是( )
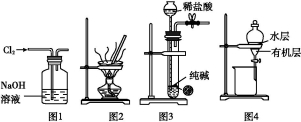
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
D
【解析】Cl2、HCl都与NaOH反应,可以选择饱和食盐水除去Cl2中的HCl,A项错;NH4Cl不稳定,受热会分解,B项错;纯碱为粉末状易溶物,不能放于带孔的板上,同时制得的CO2中会混有HCl和H2O,C项错;CCl4与水互不相溶,且CCl4的密度比水大,位于水的下层,可用分液漏斗分离,D项正确。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
元素编号 | 元素性质或原子结构 |
X | 形成的简单阳离子核外无电子 |
Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
Z | 元素在周期表的族序数等于周期序数的3倍 |
T | 同周期元素中形成的简单离子半径最小 |
下列说法正确的是( )
A.原子半径大小顺序:T>Z>Y>X
B.常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液反应生成氢气
C.X分别与Y、Z均可形成既含极性键又含非极性键的化合物
D.由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用
阿司匹林(乙酰水杨酸,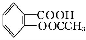 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
乙酸酐+水杨酸
 粗产品
粗产品
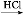
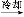
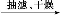 乙酰水杨酸
乙酰水杨酸
(阿司匹林) 测熔点
测熔点
主要试剂和产品的物理常数
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸酐 | 102 | 139.4(沸点) | 反应 |
乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是 。
(2)①合成阿司匹林时,最合适的加热方法是 。
②加热后冷却,未发现被冷却容器中有晶体析出,此时应采取的措施是 。
③抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是 。
(3)试剂A是 。
另一种改进的提纯方法如下:
粗产品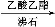
 乙酰水杨酸
乙酰水杨酸
(4)改进的提纯方法中加热回流的装置如图所示,
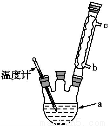
①使用温度计的目的是 。
②此种提纯方法中乙酸乙酯的作用是: ,所得产品的有机杂质要比原方案少,原因是 。