题目内容
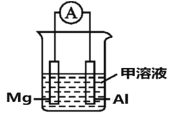
【题目】以海水为电解质的Mg-AgCl电池在军事上可用作电动鱼雷的电源,其电池反应离子方程式为:2AgCl+Mg=Mg2++2Ag+2Cl-。该电池工作时,下列说法正确的是( )

A.正、负极的质量均减少
B.电子由AgCl经外电路流向Mg
C.AgCl电极发生氧化反应
D.该装置实现了电能向化学能的转化
【答案】A
【解析】
总反应为2AgCl+Mg=Mg2++2Ag+2Cl-,原电池中负极发生氧化反应,所以Mg为负极,AgCl为正极。
A.电池正极发生反应:AgCl+e-=Ag+Cl-,有氯离子生成进入溶液,负极发生反应: Mg-2e-=Mg2+,生成镁离子进入溶液,所以正、负极质量均减少,故A正确;
B.电子经外电路由负极流向正极,即由Mg流向AgCl,故B错误;
C.AgCl为正极,发生还原反应,故C错误;
D.该装置实现了化学能向电能的转化,故D错误;
故答案为A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目