题目内容
【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是_____。非金属性最强的元素的原子结构示意图为______。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________。
(3)②③④的原子半径由大到小的顺序是_________。
(4)元素⑦的氢化物常温下和元素②的单质反应的子方程式是________。
(5)⑧的最高价氧化物对应的水化物化学式为__________。
(6)①、⑥和⑦形成的化合物的化学式为______。该化合物的化学键类型为_________。
(7)⑧⑨三种元素形成的气态氢化物最稳定的是_______。
(8)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为________。
(9)下列可以判断①和⑤金属性强弱的是_______________。
a. ①单质的熔点比⑤单质低
b. ①质软,氧化物种类比⑤多
c. ①单质与水反应,⑤单质几乎不与水反应
d. ①最高价氧化物的水化物的碱性比⑤强
【答案】Ne 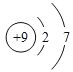 KOH K>Ca>Mg 2K+2H2O=2K+ + 2OH- + H2↑ HClO4 Na2CO3 离子键,极性共价键 HF NaOH + Al(OH)3 = NaAlO2 + 2H2O cd
KOH K>Ca>Mg 2K+2H2O=2K+ + 2OH- + H2↑ HClO4 Na2CO3 离子键,极性共价键 HF NaOH + Al(OH)3 = NaAlO2 + 2H2O cd
【解析】
由元素在周期表中位置可知:①为Na元素、②为K元素、③为Mg元素、④为Ca元素、⑤为Al元素、⑥为C元素、⑦为O元素、⑧为Cl元素、⑨为Br元素、⑩为Ar元素、为F元素,结合元素周期律以及元素的性质进行答题。
由分析可知:①为Na元素、②为K元素、③为Mg元素、④为Ca元素、⑤为Al元素、⑥为C元素、⑦为O元素、⑧为Cl元素、⑨为Br元素、⑩为Ar元素、为F元素。
(1)稀有气体Ar的化学性质最不活泼,同一周期自左向右非金属性逐渐增强,同一主族自上而下非金属性逐渐减弱,所以上述元素中F的非金属性最强,其原子结构示意图为: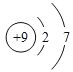 ,故答案为:Ar,
,故答案为:Ar,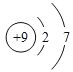 。
。
(2)①②⑤中K的金属性最强,故KOH的碱性最强,故答案为:KOH。
(3)同一周期自左向右原子半径逐渐减小,同一主族原子半径逐渐增大,所以原子半径由大到小的顺序是:K>Ca>Mg,故答案为:K>Ca>Mg。
(4)元素⑦的氢化物为H2O,该氢化物常温下和K反应生成氢氧化钾与氢气,离子方程式为:2K+2H2O=2K++2OH-+H2↑,故答案为:2K+2H2O=2K++2OH-+H2↑。
(5)⑧为Cl元素,氯元素的最高价氧化物对应的水化物为HClO4,故答案为:HClO4。
(6)①为Na元素、⑥为C元素、⑦为O元素,由Na、C、O三种元素形成的化合物为Na2CO3,Na2CO3中钠离子和碳酸根离子之间形成离子键,碳酸根中C原子与O原子之间形成极性共价键,故答案为:Na2CO3;离子键,极性共价键。
(7)⑧为Cl元素、⑨为Br元素、为F元素,同一主族元素的非金属性逐渐减弱,则F的非金属性最强,非金属性越强,形成的气态氢化物越稳定,所以⑧⑨三种元素形成的气态氢化物最稳定的是HF,故答案为:HF。
(8)①和⑤最高价氧化物对应的水化物分别为氢氧化钠、氢氧化铝,二者反应生成偏铝酸钠与水,反应方程式为:NaOH+Al(OH)3=NaAlO2+2H2O,故答案为:NaOH+Al(OH)3=NaAlO2+2H2O。
(9)a.金属性强弱与金属单质的熔点高低没有关系,故a错误;
b.金属性强弱与硬度、氧化物种类没有关系,故b错误;
c.金属性越强,其单质越容易与水反应,①单质与水反应,⑤单质几乎不与水反应,说明钠的金属性比铝强,故c正确;
d.金属性越强,最高价氧化物的水化物的碱性越强,①最高价氧化物的水化物的碱性比⑤强,说明钠的金属性比铝强,故d正确。
故答案为:cd。