题目内容
11.分类方法在化学学科的发展中起到了非常重要的作用.下列分类标准合理的是( )①根据碳酸钠溶于水呈碱性,碳酸钠既属于盐,又属于碱.
②根据反应前后是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液
④根据反应中的热效应将化学反应分为放热反应和吸热反应.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ③④ |
分析 ①碱和盐的分类是根据化合物电离出的离子的类别来分的,不是根据水溶液的酸碱性;
②氧化还原反应和非氧化还原反应的区别是否存在元素化合价的变化;
③溶液、胶体和浊液的本质区别是分散质微粒直径的大小不同;
④化学反应伴随吸热、放热,根据反应的热效应可以将反应分类.
解答 解:①碱和盐的分类是根据化合物电离出的离子的类别来分的,不是根据水溶液的酸碱性,碳酸钠溶于水呈碱性,碳酸钠仍属于盐,不属于碱,故错误;
②氧化还原反应和非氧化还原反应的区别是否存在元素化合价的变化,根据反应前后是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应,故正确;
③根据分散质微粒直径的大小不同将分散系分为溶液、胶体和浊液,故错误;
④化学反应伴随吸热、放热,根据反应的热效应将化学反应分为放热反应和吸热反应,故正确.
故选B.
点评 本题考查物质的分类,注意分类的依据和标准,题目较基础,难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
2.下列叙述不正确的是( )
| A. | 10mL O2与10mL CO2含有相同的分子数 | |
| B. | 0.5 mol H2O与0.5 mol CO含有相同的分子数 | |
| C. | 同温同压下,10mL N2和10mL NO含有相同的原子数 | |
| D. | 1 mol Fe和1 mol Cu在常温下所含的原子数相同,但体积不同 |
19.下列关于碱金属的主要性质说法正确的是( )
| A. | 单质的密度都很小,属于轻金属,且随核电荷数的增加依次增大 | |
| B. | 单质的熔点都很低,导电性、导热性都很好,如液态钠可作核反应堆的传热介质 | |
| C. | 单质与氧气反应时都只能生成氧化物或过氧化物 | |
| D. | 在Na、K、Rb三种单质中,Rb的熔点最高 |
6.已知:C(s)+O2(g)═CO2(g)△H1CO2(g)+C (s)═2CO(g)+H2(g)△H2
2CO(g)+O2(g)═2CO2(g)△H 3 4Fe(s)+3O2(g)═2Fe2O3(s)△H4
Fe2O3(s)+3CO(g)═3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变判断不正确的是( )
2CO(g)+O2(g)═2CO2(g)△H 3 4Fe(s)+3O2(g)═2Fe2O3(s)△H4
Fe2O3(s)+3CO(g)═3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变判断不正确的是( )
| A. | △H1<0,△H3<0 | B. | △H4<0,△H2>0 | C. | 3△H3═△H4+2△H5 | D. | △H3═△H1+△H2 |
20.下列实验中不需要用到玻璃棒的是( )
| A. | 萃取 | B. | 溶解 | C. | 蒸发 | D. | 过滤 |
19.苹果酸的钠盐(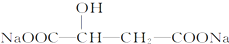 )可作为调味剂、缓冲剂、保水剂以及防腐保鲜剂,广泛应用于饮料、肉制品、口服液等.有关说法错误是( )
)可作为调味剂、缓冲剂、保水剂以及防腐保鲜剂,广泛应用于饮料、肉制品、口服液等.有关说法错误是( )
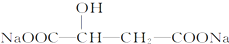 )可作为调味剂、缓冲剂、保水剂以及防腐保鲜剂,广泛应用于饮料、肉制品、口服液等.有关说法错误是( )
)可作为调味剂、缓冲剂、保水剂以及防腐保鲜剂,广泛应用于饮料、肉制品、口服液等.有关说法错误是( )| A. | 苹果酸的酸性强于醋酸 | |
| B. | 分别对苹果酸、苹果酸钠溶液微热,溶液的pH均增大 | |
| C. | 苹果酸在一定条件下发生消去反应可生成HOOCCH═CHCOOH | |
| D. | 苹果酸在一定条件下发生取代反应可生成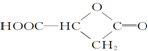 |
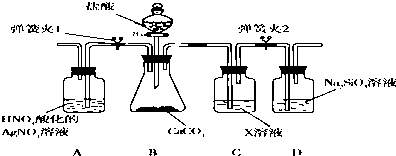
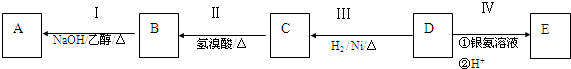
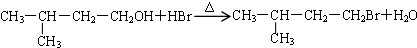 ;
; ;
; .
.