题目内容
2.下列事实能说明金属性Na>Mg的是( )| A. | Na能与冷水反应,而Mg不能 | |
| B. | Na最外层有一个电子,Mg最外层有2个电子 | |
| C. | 碱性NaOH<Mg(OH)2 | |
| D. | Na能从MgCl2 的溶液中把Mg置换出来 |
分析 利用金属单质之间的置换反应、失去电子的难易程度、金属对应阳离子的氧化性、与水或酸反应的难易程度、金属的最高价氧化物对应水化物的碱性等来比较金属性的强弱.
解答 解:A、Na能与冷水反应,而Mg不能,说明金属钠的活泼性强于金属镁,故A正确;
B、元素最外层电子数的多少不能证明金属的活泼性强弱,故B错误;
C、根据金属元素最高价氧化物对应水化物的碱性可以判断元素金属性的强弱,碱性NaOH<Mg(OH)2,能说明金属性Na>Mg,故C错误;
D、Na不能从MgCl2 的溶液中把Mg置换,而是金属钠优先和水之间反应,故D错误.
故选A.
点评 本题考查金属性的比较,明确常见的金属性比较的方法即可解答,注意B选项都是学生解答中的易错点,注意铁离子的氧化性较强,利用实例来说明问题.

练习册系列答案
相关题目
12.化学与人类生活密切相关.下列说法正确的是( )
| A. | 淀粉、脂肪和蛋白质都是人体必需的高分子化合物 | |
| B. | 汽油、柴油和植物油都是碳氢化合物 | |
| C. | 高压聚乙烯是无毒高分子化合物,可用作食品包装袋等薄膜制品 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
10.下列实验不能获得成功的是( )
①用甲烷气体通入碘水制碘甲烷
②甲烷和溴蒸气混合光照制取纯净的一溴甲烷
③用酒精灯加热甲烷气体制取炭黑和氢气.
①用甲烷气体通入碘水制碘甲烷
②甲烷和溴蒸气混合光照制取纯净的一溴甲烷
③用酒精灯加热甲烷气体制取炭黑和氢气.
| A. | 只有① | B. | 只有③ | C. | 只有② | D. | ①②③ |
17.类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其是否正确.下列几种类推结论中正确的是( )
| A. | 由2Cu+O2$\frac{\underline{\;△\;}}{\;}$2CuO可推出同族的硫也有Cu+S$\frac{\underline{\;△\;}}{\;}$CuS | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | Na能与水反应生成H2,K、Ca也能与水反应生成H2 | |
| D. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
14.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 等物质的量的N2和CO所含分子数均为NA | |
| B. | 1.7 g H2O2中含有的电子数为0.9NA | |
| C. | 标准状况下,22.4L空气含有NA个单质分子 | |
| D. | 1mol•L-1NaCl溶液含有NA个Na+ |
11.实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是( )
| A. | 950mL 容量瓶 | B. | 500mL容量瓶 | ||
| C. | 1000mL 容量瓶 | D. | 任意规格的容量瓶 |

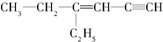 ,分子中饱和碳原子数为4,可能在同一平面上的碳原子数最多为8.
,分子中饱和碳原子数为4,可能在同一平面上的碳原子数最多为8.