题目内容
常温下,0.1 mol·L-1的HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述中正确的是
A.0.01mol·L-1 HA的溶液中c(H+)=1×10-4 mol·L-1
B.pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C.pH=3的HA溶液与pH=11的NaO H溶液按体积比l:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+)
D.浓度均为0.1 mol·L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-)
A.0.01mol·L-1 HA的溶液中c(H+)=1×10-4 mol·L-1
B.pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C.pH=3的HA溶液与pH=11的NaO H溶液按体积比l:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+)
D.浓度均为0.1 mol·L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-)
C
试题分析:根据题意知,常温下,0.1 mol·L-1的HA溶液中c(OH-)/c(H+)=1×10-8,而Kw=c(H+)c(OH-)=10-14,则溶液中氢离子浓度为0.001mol·L-1,则HA为弱酸; A、HA为弱酸,加水稀释,促进电离,0.01mol·L-1 HA的溶液中c(H+)>1×10-4 mol·L-1,错误;B、HA为弱酸,pH=3的HA溶液与pH=11的NaOH溶液等体积混合后HA远远过量,所得溶液中c(A-)>c(Na+)>c(H+)>c(OH-),错误;C、根据电荷守恒判断,pH=3的HA溶液与pH=11的NaO H溶液按体积比l:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+),正确;D、浓度均为0.1 mol·L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则HA的电离程度大于NaA,则c(H+)- c(OH-)-<c(A-)-c(HA),错误。

练习册系列答案
相关题目
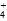 与Cl-浓度比为1∶1的溶液,可在NH4Cl溶液中加入( )
与Cl-浓度比为1∶1的溶液,可在NH4Cl溶液中加入( ) NH3·H2O+H+
NH3·H2O+H+