题目内容
5.某短周期元素最低负价为-2价,该元素的离子跟其核外电子排布相同的离子形成的化合物是( )| A. | K2S | B. | MgO | C. | MgS | D. | H2O2 |
分析 某短周期元素最低负价为-2价,根据最高正价+|最低负价|=8,可知该元素第VIA族,应为S元素或O元素,硫离子核外有18个电子,所以另一离子应含有18个电子,或氧离子核外有10个电子,所以另一离子应含有10个电子.据此判断.
解答 解:某短周期元素最低负价为-2价,根据最高正价+|最低负价|=8,可知该元素第VIA族,应为S元素或O元素,硫离子核外有18个电子,所以另一离子应含有18个电子,或氧离子核外有10个电子,所以另一离子应含有10个电子,
A.硫离子与钾离子核外电子排布相同,故A正确;
B.氧离子与镁离子核外电子排布相同,故B正确;
C.硫离子与镁离子核外电子排布不相同,故C错误;
D.H2O2不是离子化合物,属于共价化合物,故D错误;.
故选:AB.
点评 本题考查元素的推断与物质的组成,推出元素为S元素是解答本题的关键,学生应学会利用原子结构来推断元素.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
13.相同温度、相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g)?3W(g)+2Z(g)△H=-Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表:
下列说法正确的是( )
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出akJ/mol | ||
| 乙 | 1mol | 1mol | 放出b kJ/mol | ||
| 丙 | 2mol | 2mol | 放出c kJ/mol | ||
| 丁 | 3mol | 2mol | 吸收d kJ/mol |
| A. | c+d<Q | |
| B. | 平衡时,甲、丁容器中X、W的转化率之和等于1 | |
| C. | 平衡时丙容器中Z的物质的量浓度最大 | |
| D. | X的转化率为:甲<乙<丙 |
10.稀土硼化物广泛用于雷达、航空航天、冶金、环保等多个高科技领域.下列元素与硼元素处于同一主族的是( )
| A. | Be | B. | O | C. | Mg | D. | Al |
17.化学是以实验为基础的自然科学,化学实验操作中必须十分重视安全问题和环境保护问题.下列实验问题处理方法正确的是( )
| A. | 做氢气还原氧化铜的实验时先加热再通氢气 | |
| B. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| C. | 浓硫酸不小心沾到皮肤上,立刻用NaOH溶液洗涤 | |
| D. | 实验室制取气体时应先检查装置的气密性 |
14.下面说法正确的是( )
| A. | 含有羟基的化合物一定属于醇类 | |
| B. | 酚和醇都含有羟基,但其化学性质不完全相同 | |
| C. | 分子中含有苯环和羟基的化合物一定是酚 | |
| D. | Na2SO3、Na2O2、苯酚久置于空气中,颜色均有变化 |

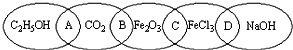 如图为五个椭圆交叉构成的图案,椭圆内分别写C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题:
如图为五个椭圆交叉构成的图案,椭圆内分别写C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题: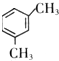 .
.