题目内容
【题目】某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2。
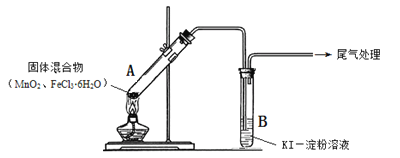
实验操作和现象:
操 作 | 现 象 |
点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾是 ,形成白雾的原因是 。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
通过该实验说明现象ⅱ中黄色气体含有 。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
① 实验b检出的气体使之变蓝,反应的离子方程式是________________。实验证实推测成立。
② 溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是 。
(4)为进一步确认黄色气体是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI-淀粉溶液替换为NaBr溶液;检验Fe2+ 。
现象如下:
方案1 | B中溶液变为蓝色 |
方案2 | B中溶液呈浅橙红色;未检出Fe2+ |
①方案1的C中盛放的试剂是 。
②方案2中检验Fe2+ 的原因是 。
③综合方案1、2的现象,说明选择NaBr溶液的依据是 。
(5)将A中产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是 。
【答案】(1)盐酸小液滴(盐酸酸雾)
加热时,FeCl3发生水解反应产生HCl,HCl挥发出来遇水蒸气形成白雾
(2)FeCl3
(3)①2Fe3++2I-![]() I2+2Fe2+②在KI-淀粉溶液中滴加少量盐酸,放置在空气中,观察溶液能否变蓝
I2+2Fe2+②在KI-淀粉溶液中滴加少量盐酸,放置在空气中,观察溶液能否变蓝
(4)①饱和食盐水
②通过未检测出Fe2+证明,说明是Cl2将Br-氧化为Br2而不是Fe3+氧化的,证明了黄色气体中一定含有Cl2
③氧化性强弱顺序:Cl2>Br2>Fe3+
(5)2FeCl3·6H2O+MnO2![]() Fe2O3+MnCl2+Cl2↑+2HCl↑+11H2O
Fe2O3+MnCl2+Cl2↑+2HCl↑+11H2O
【解析】
试题分析:(1)FeCl3·6H2O加热水解生成氢氧化铁和氯化氢,HCl挥发出来遇水蒸气形成白雾,白雾是盐酸小液滴;(2)用KSCN溶液检验,溶液均变红,说明一定含有FeCl3;(3)FeCl3与碘化钾反应的方程式2Fe3++2I-![]() I2+2Fe2+;②在KI-淀粉溶液中滴加少量盐酸,放置在空气中,观察溶液能否变蓝;(4)①方案1需要除去氯气中的氯化铁,所以的C中盛放的试剂是饱和食盐水;②方案2中检验Fe2+的原因是通过未检测出Fe2+证明,说明是Cl2将Br-氧化为Br2而不是Fe3+氧化的,证明了黄色气体中一定含有Cl2;③氧化性强弱顺序:Cl2>Br2>Fe3+,氯气能氧化Br-、Fe3+不能氧化化Br-。(5)将A中产物分离得到Fe2O3和MnCl2,可知二氧化锰氧化氯离子生成氯气,反应方程式2FeCl3·6H2O+MnO2
I2+2Fe2+;②在KI-淀粉溶液中滴加少量盐酸,放置在空气中,观察溶液能否变蓝;(4)①方案1需要除去氯气中的氯化铁,所以的C中盛放的试剂是饱和食盐水;②方案2中检验Fe2+的原因是通过未检测出Fe2+证明,说明是Cl2将Br-氧化为Br2而不是Fe3+氧化的,证明了黄色气体中一定含有Cl2;③氧化性强弱顺序:Cl2>Br2>Fe3+,氯气能氧化Br-、Fe3+不能氧化化Br-。(5)将A中产物分离得到Fe2O3和MnCl2,可知二氧化锰氧化氯离子生成氯气,反应方程式2FeCl3·6H2O+MnO2![]() Fe2O3+MnCl2+Cl2↑+2HCl↑+11H2O。
Fe2O3+MnCl2+Cl2↑+2HCl↑+11H2O。