题目内容
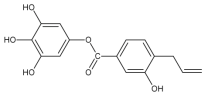
【题目】一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
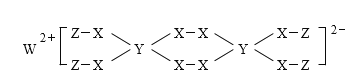
A.工业上通过电解熔融的WX来制得W
B.W、X对应的简单离子半径顺序为:W>X
C.该漂白剂中各元素均满足8电子稳定结构
D.Y的最高价氧化物对应水化物为弱酸
【答案】D
【解析】
从图中可以看出,Y显4价,说明最外层电子数为4,X显2价,最外层电子数为6,W显+2价,说明它是第ⅡA族的金属元素,所以Z为氢(H);由“W、X对应的简单离子核外电子排布相同”,可确定W为镁(Mg),X为氧(O),从而得出Y为碳(C)。
A.工业上利用电解熔融MgCl2的方法制镁,A不正确;
B.W(Mg)、X(O)对应的简单离子半径顺序为:O2->Mg2+,B不正确;
C.该漂白剂中氢(H)元素不满足8电子稳定结构,C不正确;
D.Y为碳(C),它的最高价氧化物对应水化物H2CO3为弱酸,D正确;
故选D。

 一本好题口算题卡系列答案
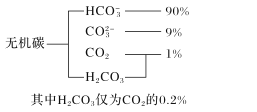
一本好题口算题卡系列答案【题目】轻质碳酸钙是一种广泛应用的工业填料,主要用于塑料、造纸、橡胶和涂料等。工业上以磷石膏(主要成分为CaSO4,杂质主要是SiO2、FeO、Fe2O3、Al2O3等)为原料制备轻质碳酸钙。已知碳酸钙的溶解度比硫酸钙的溶解度小,在一定温度下,钙离子开始沉淀的pH值为12.3,氢氧化铝开始溶解的pH值为12.0,其他金属离子形成氢氧化物沉淀的相关pH的范围如下:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Al3+ | 3.0 | 4.7 |
制备流程如图:

请问答:
(1)以下说法正确的是__。
A.溶解的过程中,可以用盐酸代替硝酸
B.滤渣1的主要成分是SiO2,滤渣2的上要成分是Fe(OH)3、Al(OH)3
C.转化时,可以先通氨气至饱和后再通过量二氧化碳,以提高钙离子的转化率
D.转化时可以适当加热,以加快反应速率
E.洗涤时可以采用滤液3
(2)调节溶液pH范围时,最佳的pH范围是__,理由是__。
(3)碳酸钙产品中钙含量的测定:
用电子天平准确称量产品2.000g于干净的烧杯中,滴加2mol/L的盐酸恰好完全溶解,加蒸馏水继续蒸发除去过量的酸至pH=6~7,转移至250mL的容量瓶中,定容摇匀。用移液管准确移取25.00mL溶液于锥形瓶中,加入NaOH溶液10mL,摇匀,加入钙指示剂30mg,用已标定的EDTA(乙二胺四乙酸,可以表示为H4Y)标准溶液进行滴定。
已知:Ca2++Y4-=[CaY]2-,测定数据如下:
待测产品溶液体积(mL) | 消耗EDTA标准溶液体积(mL) | EDTA标准溶液的浓度(mol) | |
1 | 25.00 | 14.90 | 0.1121 |
2 | 25.00 | 16.72 | 0.1121 |
3 | 25.00 | 15.00 | 0.1121 |
4 | 25.00 | 15.10 | 0.1121 |
①进行整个滴定操作实验的过程中,下列操作方法正确的是__。
A.使用移液管移取溶液的时候,移液管尖嘴不能接触容器壁
B.滴定管水洗后,需要用标准溶液润洗3次,再排出气泡,使液面位于“0”刻度或“0”刻度以下
C.滴定管调液面后,需静置1~2min,再进行读取刻度数据进行记录
D.电子天平读数时,两边侧面应同时处于打开状态,使空气保持流通
②该产品中钙元素的质量分数为__(保留两位有效数字),若滴定结束时仰视读数,则测定的结果__(填“偏大”、“偏小”或“无影响”)。