题目内容
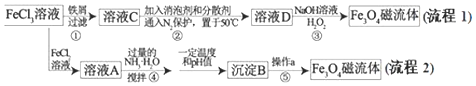
【题目】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域.如图是制备纳米![]() 磁流体的两种流程:
磁流体的两种流程:
![]() 分析流程图中的两种流程,其中______
分析流程图中的两种流程,其中______![]() 填“流程1”、“流程2”
填“流程1”、“流程2”![]() 所有反应不涉及氧化还原反应.步骤
所有反应不涉及氧化还原反应.步骤![]() 反应的离子方程式为______.
反应的离子方程式为______.
![]() 步骤
步骤![]() 保持
保持![]() 的方法是______.
的方法是______.
![]() 步骤
步骤![]() 中加入的
中加入的![]() 电子式是______,步骤
电子式是______,步骤![]() 制备
制备![]() 磁流体的化学方程式为______.
磁流体的化学方程式为______.
![]() 流程2中
流程2中![]() 和
和![]() 制备
制备![]() 磁流体,理论上
磁流体,理论上![]() 和
和![]() 物质的量之比为______
物质的量之比为______![]() 己知沉淀B为四氧化三铁.步骤
己知沉淀B为四氧化三铁.步骤![]() 中操作a具体的步骤是______.
中操作a具体的步骤是______.
![]() 利用
利用![]() 可测定
可测定![]() 磁流体中的
磁流体中的![]() 含量.若
含量.若![]() 磁流体与
磁流体与![]() 充分反应消耗了
充分反应消耗了![]() 的
的![]() 标准溶液100mL,则磁流体中含有
标准溶液100mL,则磁流体中含有![]() 的物质的量为______mol.
的物质的量为______mol.
【答案】流程2 ![]() 水浴加热
水浴加热 ![]()
![]() 2:l 过滤、洗涤、干澡
2:l 过滤、洗涤、干澡 ![]()
【解析】
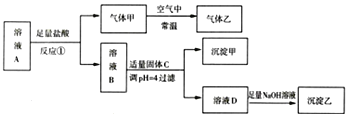
氯化铁溶液中加入铁屑过滤得到溶液C为氯化亚铁溶液,加入消泡剂和分散剂通入氮气保护置于50°C容器中得到溶液D,加入氢氧化钠溶液和过氧化氢得到磁性氧化铁,氯化铁和氯化亚铁混合溶液A加入过量氨水搅拌在一定温度和pH条件下生成沉淀B为四氧化三铁,经过滤、洗涤、干澡可得到磁性氧化铁;
(1)流程1中存在铁和氯化铁反应为氧化还原反应,流程2中发生的是复分解反应;步骤①反应为铁还原铁离子生成亚铁离子;
(2)温度低于100°C的加热条件可以用水浴加热;
(3)过氧化氢为共价化合物,具有氧化性,在氢氧化钠溶液中和氯化亚铁反应生成四氧化三铁、氯化钠和水;
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,四氧化三铁可以看做Fe2O3FeO,结合元素守恒判断;
(5)用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量,K2Cr2O7被还原成Cr3+,依据反应的离子方程式Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O的定量关系计算。
![]() 氯化铁和铁反应生成醋酸氯化亚铁,反应的离子方程式
氯化铁和铁反应生成醋酸氯化亚铁,反应的离子方程式![]() ,所以流程1中一定存在氧化还原反应,流程2中,溶液A为氯化铁和氯化亚铁的混合溶液加入氨水生成氢氧化铁、氢氧化亚铁,经过操作最后得到四氧化三铁,过程中无元素化合价变化,流程2无氧化还原反应,步骤
,所以流程1中一定存在氧化还原反应,流程2中,溶液A为氯化铁和氯化亚铁的混合溶液加入氨水生成氢氧化铁、氢氧化亚铁,经过操作最后得到四氧化三铁,过程中无元素化合价变化,流程2无氧化还原反应,步骤![]() 反应为铁还原铁离子生成亚铁离子,反应的离子方程式为:
反应为铁还原铁离子生成亚铁离子,反应的离子方程式为:![]() ;
;
![]() 步骤
步骤![]() 中,若要保持
中,若要保持![]() 的温度,操作方法是:将反应装安放在水浴中加热;
的温度,操作方法是:将反应装安放在水浴中加热;
![]() 过氧化氢为共价化合物,电子式为
过氧化氢为共价化合物,电子式为![]() ,步骤
,步骤![]() 制备
制备![]() 磁流体,是过氧化氢在氢氧化钠溶液中和氯化亚铁反应生成四氧化三铁、氯化钠和水,反应的化学方程式为:
磁流体,是过氧化氢在氢氧化钠溶液中和氯化亚铁反应生成四氧化三铁、氯化钠和水,反应的化学方程式为:![]() ;
;
![]() 流程2中
流程2中![]() 和
和![]() 制备
制备![]() 磁流体,四氧化三铁可以看做
磁流体,四氧化三铁可以看做![]() ,理论上
,理论上![]() 和
和![]() 物质的量之比为2:1,氯化铁和氯化亚铁混合溶液A加入过量氨水搅拌在一定温度和pH条件下生成沉淀B为四氧化三铁,经过滤、洗涤、干澡可得到磁性氧化铁;
物质的量之比为2:1,氯化铁和氯化亚铁混合溶液A加入过量氨水搅拌在一定温度和pH条件下生成沉淀B为四氧化三铁,经过滤、洗涤、干澡可得到磁性氧化铁;
![]() 反应的离子方程式为
反应的离子方程式为![]() ,
,![]() ,则磁流体中含有
,则磁流体中含有![]() 的物质的量为
的物质的量为![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案