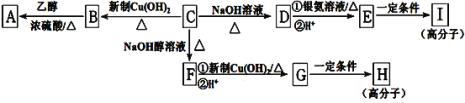
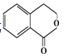
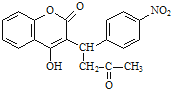
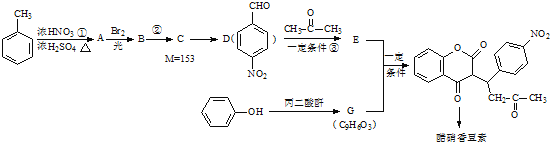
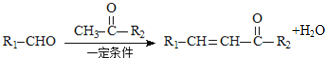题目内容
【题目】大庆市某中学化学实验小组在实验室鉴定某无色溶液.已知溶液中的溶质仅由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种组成.取该溶液进行如下实验:
中的若干种组成.取该溶液进行如下实验:
![]() 取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
![]() 在
在![]() 所得溶液中加入过量
所得溶液中加入过量![]() 溶液,有气体生成,同时产生白色沉淀甲;
溶液,有气体生成,同时产生白色沉淀甲;
![]() 在
在![]() 所得溶液中加入过量
所得溶液中加入过量![]() 溶液并加热也有气体生成,同时产生白色沉淀乙
溶液并加热也有气体生成,同时产生白色沉淀乙
则下列离子在原溶液中一定存在的有![]()
A.![]() 、
、![]() 、
、![]() B.
B.![]() 、
、![]() 、
、![]() 、
、![]() 、
、
C.![]() 、
、![]() 、
、![]() D.
D.![]() 、
、![]() 、
、![]() 、
、![]()
【答案】A
【解析】
原溶液无色,说明该溶液中不存在MnO4-。实验(1)加入盐酸有气体生成,所以溶液中含有CO32-,则溶液中不存在Ag+、Ca2+、Al3+;
实验(2)产生的气体是(1)过量的盐酸电离生成的H+与HCO3-反应生成的CO2,沉淀只可能是Al3+与HCO3-反应生成的Al(OH)3,则实验(1)中必有AlO2-与过量盐酸反应生成Al3+,而原溶液存在AlO2-时,NH4+必然不存在;
实验(3)的气体和沉淀都可能是(2)过量的NH4HCO3与Ba(OH)2反应生成的NH3和BaCO3,所以SO42-是否存在无法判断。综上所述,原溶液中一定不存在Ag+、Ca2+、Al3+、MnO4- 、NH4+,则仅剩的K+一定存在于溶液中,则原溶液一定存在AlO2-、CO32-和K+,而SO42-无法判断。
答案选A。

 阅读快车系列答案
阅读快车系列答案【题目】某工业废水中仅含下表离子中的5种:
阳离子 |
|
阴离子 |
|
某同学欲探究废水的组成,进行了如下实验:
Ⅰ![]() 取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
Ⅱ![]() 向Ⅰ中所得的溶液中加入
向Ⅰ中所得的溶液中加入![]() 溶液,有白色沉淀生成.
溶液,有白色沉淀生成.
下列推断不正确的是![]()
A.溶液中一定含有的离子是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]()
B.Ⅰ中加入盐酸生成无色气体的离子方程式是![]()
C.原溶液中的![]() 、
、![]() 、
、![]() 存在与否无法确定
存在与否无法确定
D.Ⅱ中产生白色沉淀的离子方程式是