题目内容
5.今有KBr、NaBr的混合物5g,和过量AgNO3溶液反应后,得到溴化银8.4g.求混合物中两种盐各有多少克?(KBr3g,NaBr2g)分析 根据n=$\frac{m}{M}$计算出生成溴化银的物质的量,然后设出KBr、NaBr的物质的量,分别根据混合物质量、生成溴化银的物质的量列式计算即可.
解答 解:8.4gAgBr的物质的量为:$\frac{8.4g}{188g/mol}$≈0.0447mol,
设混合物中含有KBr、NaBr的物质的量分别为x、y,
则:$\left\{\begin{array}{l}{119x+103y=5}\\{x+y=0.0447}\end{array}\right.$,
解得:x=0.0247mol、y=0.0200mol,
则混合物中KBr的质量为:119g/mol×0.0247mol≈3.0g,NaBr的质量为:5g-3g=2g,
答:混合物中溴化钾的质量为3g,溴化钠的质量为2g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的灵活运用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
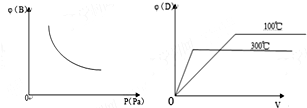
15.在容积固定的密闭容器中,进行下列反应A(g)+B(g)?2C(?)+D(g),此反应符合下列两个图象(其中φ代表物质的百分含量),则下列判断正确的是( )

| A. | 物质C不可能为气态 | |
| B. | 正反应为吸热反应 | |
| C. | 该反应,升高温度平衡正向移动 | |
| D. | 300℃下该反应到达平衡状态后,迅速充入He,平衡正向移动 |
16.下列各组混合物中,总质量一定时,二者以不同比例混合,完全燃烧时生成CO2的质量不一定的是( )
| A. | 甲烷、辛醛 | B. | 乙炔、乙烯 | C. | 乙烯、庚烯 | D. | 苯、甲苯 |
10.下列叙述不正确的是( )
| A. | 纯水也是一种电解质 | |
| B. | 无论是酸性、中性还是碱性稀溶液,只要温度恒定,c(H+)×c(OH-)是一个常数 | |
| C. | 一定温度下,0.1mol•L-1的磷酸溶液中H+主要来自于酸的第一步电离 | |
| D. | 强碱溶液中不存在H+ |
4.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,4v正(O2)=5v逆(NO) | |
| D. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) |
1.下列说法中不属于“雾霾”等灾害性天气治理措施的是( )
| A. | 外出时使用PM2.5口罩,减少有害物质的吸入 | |
| B. | 改燃煤为燃气,可减少废气中SO2等有害物质的量 | |
| C. | 利用太阳能、潮汐能、风力发电,以获取清洁能源 | |
| D. | 使用“乙醇汽油”,减少汽车尾气中有害气体的排放 |