题目内容
6.NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,22.4LCH4中含有原子数目约为NA | |
| B. | 标准状况下,NA个H2O分子的体积约为22.4L | |
| C. | 常温常压下,NA个D2O分子的质量约为20g | |
| D. | 1L 0.5mol/L AlCl3溶液中含有的Al3+数目约为NA |
分析 A.1个甲烷分子含有5个原子;
B.气体摩尔体积使用对象为气体;
C.依据m=nM计算;
D.铝离子为弱碱阳离子,在水溶液中部分发生水解.
解答 解:A.标准状况下,22.4LCH4的物质的量为1mol,含有原子个数约为5NA,故A错误;
B.标况下水是液体,不能使用气体摩尔体积,故B错误;
C.常温常压下,NA个D2O分子的物质的量为1mol,质量为1mol×20g/mol=20g,故C正确;
D.铝离子为弱碱阳离子,在水溶液中部分发生水解,所以1L 0.5mol/L AlCl3溶液中含有的Al3+数目小于NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,明确以物质的量为中心的相关计算公式即可解答,注意气体摩尔体积使用对象和条件,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
16. 如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
 如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
如图所示,锥形瓶中盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,震荡,过一会儿可见小气球a鼓起.气体X和液体Y不可能是( )| A. | X是NH3,Y是水 | B. | X是CO2,Y是饱和NaHCO3浓溶液 | ||
| C. | X是SO2,Y是NaOH溶液 | D. | X是HCl,Y是NaNO3稀溶液 |
1.如图为铜锌原电池示意图,下列说法中正确的是( )
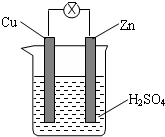

| A. | 烧杯中溶液逐渐呈蓝色 | B. | 锌片逐渐溶解 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能够将电能转化为化学能 |
18.某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物
测定生成气体的体积
方案Ⅱ:铜铝混合物
测定剩余固体的质量
下列有关判断中不正确的是( )
方案Ⅰ:铜铝混合物
| 足量溶液A |
| 充分反应 |
方案Ⅱ:铜铝混合物
| 足量溶液B |
| 充分反应 |
下列有关判断中不正确的是( )
| A. | 溶液A和B均可以是盐酸 | B. | 溶液A和B均可以是NaOH溶液 | ||
| C. | 溶液A和B均可选用稀硝酸 | D. | 实验室中方案Ⅱ更便于实施 |
15.有一包固体混合物,其中含有硝酸银,硝酸铜,硝酸镁及铁粉,加入足量的水过滤.下列描述的情形不可能存在的是( )
| A. | 滤纸上有Ag,Cu,Fe滤液中有Fe2+,Mg2+ | |
| B. | 滤纸上有Ag,滤液中有Fe2+,Cu2+,Mg2+,Ag+ | |
| C. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+ | |
| D. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+,Ag+ |
16.在NaClO中加入浓盐酸产生黄绿色气体X,在Na2SO3中加入稀H2SO4产生无色气体Y,下列对X、Y的叙述中错误的是( )
| A. | 将X、Y分别通入品红溶液中,均使品红溶液褪色 | |
| B. | 将X、Y分别通入氢硫酸中,只有Y能产生沉淀 | |
| C. | 等物质的量的X、Y同时通入品红溶液中,品红溶液不褪色 | |
| D. | 等物质的量的X、Y同时通入BaCl2溶液中,有沉淀产生 |