题目内容
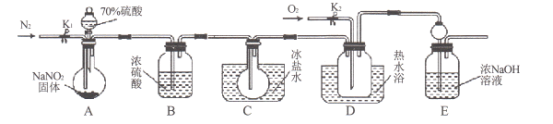
【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。


(1)仪器D的名称是________。安装F中导管时,应选用图2中的________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O,为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜________(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是_____________________________________________________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为________________________________________________________________________。
在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是
________________________________________________________________________。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是________________,原因是________________________________________________________________________。

图3
【答案】锥形瓶 b 慢 吸收Cl2 4H++5ClO![]() ===Cl-+4ClO2↑+2H2O 验证是否有ClO2生成 稳定剂Ⅱ 稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度
===Cl-+4ClO2↑+2H2O 验证是否有ClO2生成 稳定剂Ⅱ 稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度
【解析】
A装置制取ClO2,C装置吸收杂质气体Cl2,D装置吸收ClO2,F装置验证是否有氯气。
(1)仪器D为锥形瓶。根据实验分析,F装置中发生气体与KI反应,所以应“长进短出”,选择装置b。
(2)若盐酸滴加速度过快,则生成ClO2的速度快,稳定剂无法充分吸收,所以滴加盐酸速度要慢。
(3)F中的颜色不变,说明没有氯气进入F中与KI反应,装置C的作用是吸收氯气。
(4)酸性条件下ClO![]() 发生歧化反应,生成Cl-和ClO2,歧化反应逆向配平;“ClO2释放实验”说明D中发生反应生成ClO2,因此F中淀粉和KI溶液是验证是否有ClO2生成,若有ClO2生成,ClO2会氧化I-生成I2,使F中的淀粉溶液变蓝色。
发生歧化反应,生成Cl-和ClO2,歧化反应逆向配平;“ClO2释放实验”说明D中发生反应生成ClO2,因此F中淀粉和KI溶液是验证是否有ClO2生成,若有ClO2生成,ClO2会氧化I-生成I2,使F中的淀粉溶液变蓝色。
(5)水果保鲜希望保鲜时间越长越好,所以选用稳定剂Ⅱ,因为其缓慢释放ClO2,能较长时间维持保鲜所需的浓度。
(1)仪器D为锥形瓶。根据实验分析,F装置中发生气体与KI反应,所以应“长进短出”,选择装置b。
正确答案:锥形瓶 b。
(2)若盐酸滴加速度过快,则生成ClO2的速度快,稳定剂无法充分吸收,所以滴加盐酸速度要慢。
正确答案:慢。
(3)F中的颜色不变,说明没有氯气进入F中与KI反应,装置C的作用是吸收氯气。
正确答案:吸收Cl2。
(4)酸性条件下ClO![]() 发生歧化反应,生成Cl-和ClO2,歧化反应逆向配平4H++5ClO
发生歧化反应,生成Cl-和ClO2,歧化反应逆向配平4H++5ClO![]() ===Cl-+4ClO2↑+2H2O;“ClO2释放实验”说明D中发生反应生成ClO2,因此F中淀粉和KI溶液是验证是否有ClO2生成,若有ClO2生成,ClO2会氧化I-生成I2,使F中的淀粉溶液变蓝色。
===Cl-+4ClO2↑+2H2O;“ClO2释放实验”说明D中发生反应生成ClO2,因此F中淀粉和KI溶液是验证是否有ClO2生成,若有ClO2生成,ClO2会氧化I-生成I2,使F中的淀粉溶液变蓝色。
正确答案:4H++5ClO![]() ===Cl-+4ClO2↑+2H2O 验证是否有ClO2生成。
===Cl-+4ClO2↑+2H2O 验证是否有ClO2生成。
(5)水果保鲜希望保鲜时间越长越好,所以选用稳定剂Ⅱ,因为其缓慢释放ClO2,能较长时间维持保鲜所需的浓度。
正确答案:稳定剂Ⅱ 稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度。

 阅读快车系列答案
阅读快车系列答案