题目内容
9.下列有关说法不正确的是( )| A. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| B. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| C. | 一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H<0,△S>0 | |
| D. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 |
分析 A.依据反应自发进行的判断依据△H-T△S<0解答;
B.根据反应可知△S>0,室温下不能自发进行,说明该反应的△H>0;
C.依据反应MgCl2(l)═Mg(l)+Cl2(g)气体系数增大,反应放热判断;
D.△H-T△S>0反应非自发进行,反应△S>0,△H>0.
解答 解:A、反应NH3(g)+HCl(g)═NH4Cl(s)气体系数减小,△S<0,在室温下可自发进行即△H-T△S<0,所以,一定满足△H<0,故A正确;
B、CaCO3(s)═CaO(s)+CO2(g)气体的量增大,△S>0,因为室温下不能自发进行,说明该反应的△H>0,故B错误;
C、反应MgCl2(l)═Mg(l)+Cl2(g)气体系数增大,反应放热,所以△H<0,△S>0,故C正确;
D、△H-T△S>0,反应非自发进行,反应△S>0,满足△H-T△S>0,则△H>0,故D正确;
故选B.
点评 本题考查了化学反应自发进行大判断依据和条件分析,注意反应是否自发进行需要焓变、熵变、温度共同决定,题目难度中等.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
19.对于物质的量相同的CH4和NH3,下列说法不正确的是( )
| A. | 可能具有相同的密度 | B. | 可能具有相同的体积 | ||
| C. | 可能具有相同的氢原子数 | D. | 一定具有相同的电子数 |
20.下列叙述正确的是( )
| A. | 1mol任何气体的体积一定是22.4L | |
| B. | 在标准状况下,体积为22.4L的物质都是1mol | |
| C. | 标准状况下,22.4L任何气体所含分子数都约为6.02×1023个 | |
| D. | 在常温时,1mol任何气体的体积不可能是22.4L |
17.不同条件下,对于工业合成氨反应:N2+3H2 ?2NH3,下列表示其反应最快的是( )
| A. | v(H2)=0.09 mol/(L•s) | B. | v(N2)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.02 mol/(L•min) | D. | v(NH3)=0.03 mol/(L•s) |
4.下列溶液中,操作对应的现象正确的是( )
| 溶液 | 操作 | 现象 | |
| A | 滴有酚酞的明矾溶液 | 加热 | 溶液颜色变深 |
| B | 滴有酚酞的氨水 | 加入少量NH4Cl固体 | 溶液颜色变浅 |
| C | 滴有酚酞的CH3COONa溶液 | 加入少量NaOH固体 | 溶液颜色变浅 |
| D | 氯化铁溶液 | 加热 | 溶液颜色变浅 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有关维生素和微量元素的叙述不正确的是( )
| A. | 合理摄入维生素C能增强对传染病的抵抗力,而且它还有解毒作用 | |
| B. | 维生素D属于典型的水溶性维生素 | |
| C. | 为减少新鲜蔬菜中的维生素C的流失,炒蔬菜的时间不能太长,炒熟即可 | |
| D. | 补充维生素D有利于人体钙的摄入 |
1.羊毛、尼龙、纯棉布分别灼烧时产生的气味如表:
则羊毛、尼龙、纯棉布分别是上述织物中的①、③、②(填写序号).
| 织物 | ① | ② | ③ |
| 灼烧时的气味 | 烧焦羽毛的气味 | 烧纸的气味 | 特殊的气味 |
18.下列说法正确的是( )
| A. | H与D、16O与18O互为同位素,H216O、D216O、H218O、D218O互为同分异构体 | |
| B. | 金刚石、石墨均为碳的同素异形体,其化学性质与物理性质均不相同 | |
| C. | 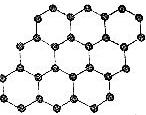 石墨烯(结构如图所示)是由碳原子构成的单层片状结构的新材料,与石墨互为同位素 | |
| D. | 由于氢原子可以形成H-(如NaH),所以有人建议可将氢元素排在元素周期表的ⅦA族 |
19.保持温度不变,向NH4Cl溶液中加入一定量的水,则( )
| A. | 溶液中各离子的浓度都减小 | B. | c(Cl-)/c(NH4+)减小 | ||
| C. | c(H+)/c(NH4+)增大 | D. | c(H+)•c(OH-)减小 |