题目内容
【题目】基础知识填空:
(1)氢氧化铁胶体制备的化学方程式_______________,所得分散系及下列物质分别用激光照射,与该分散系现象相同的是______。
A、淀粉溶液 B、澄清水 C、纳米铁 D、豆浆
(2)装置的选择:
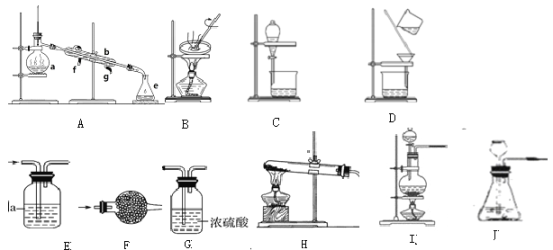
a、干燥氨气______。
b、分离植物油和水______。
c、检验CO中的是否含有CO2______。
d、分离碘和四氯化碳______。
e、实验室用氢氧化钙和氯化铵共热制氨气______。
f、实验室用稀盐酸和石制二氧化碳______。
(3)以物质的量为中心的计算
①、12.4gNa2X中含Na+0.4mol,则X的相对原子质量是______。
②、500mL质量分数为49%的硫酸溶液,密度为1.392g/cm3,则溶液的物质的量浓度为______________mol/L,其中含有SO42-的数目约为______(保留三位有效数字)。
(4)一定物质的量浓度溶液的配制:
①、实验室要配制480mL0.25mol·L-1的FeSO4溶液,需称量绿矾(FeSO4·7H2O)______g,
②、由于错误操作,使得实际浓度比所要求的偏小的是______(填写编号)。
A 称量绿矾时,左码右物
B 使用容量瓶配制溶液时,俯视液面定容,所得溶液的浓度
C 没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D 容量瓶刚用蒸馏水洗净,没有干燥
E 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F 把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
③、定容时,若加蒸馏水时不慎超过刻度线,处理方法是______。
【答案】FeCl3 + 3H2O == Fe(OH)3(胶体) + 3HClADFCEAHJ166.962.09×1024个34.8ACEF重新配制
【解析】
(1)把饱和氯化铁溶液滴入沸水中,继续加热,得到红褐色液体为氢氧化铁胶体,化学方程式:FeCl3 +3H2O == Fe(OH)3(胶体) +3HCl;胶体具有丁达尔效应,淀粉溶液、豆浆均为胶体,此两种分散系分别用激光照射,与氢氧化铁胶体分散系现象相同;而澄清水为溶液,纳米铁不属于胶体,没有丁达尔现象;综上所述,本题答案是:FeCl3 + 3H2O ==Fe(OH)3(胶体)+3HCl ;AD。
(2)a、干燥氨气用碱石灰,固体干燥剂放在球形干燥管内,选F装置;因此本题答案是:F。
b、植物油和水互不相溶,液体分层,可用分液进行分离,选C装置;因此本题答案是:C。
c、CO2能够与石灰水反应,而一氧化碳不与石灰水反应,选E装置;因此本题答案是:E。
d、碘和四氯化碳互溶,不分层,但是二者沸点不同,可以采用蒸馏进行分离,选A 装置;因此本题答案是:A。
e、实验室用氢氧化钙和氯化铵共热制氨气,为固体和固体加热反应制备气体,应用H装置;因此本题答案是:H。
f、实验室用稀盐酸和石制二氧化碳,固体和液体反应制备气体,不需要加热,应用J装置;因此本题答案是:J。
(3)①X的原子量为R,Na2X的物质的量为12.4/ (23×2+R)mol,含有Na+0.4mol,因此2×12.4/(23×2+R)=0.4,R=16;则X的相对原子质量是16;因此本题答案:16。
②、根据公式:c=1000×ρ×ω/M,溶液的物质的量浓度=1000×1.392×49%/98=6.96mol/L,500mL该溶液中含有SO42-的量为:0.5×6.96=3.48mol, 含有SO42-数目约为3.48×6.02×1023=2.09×1024个;综上所述,本题答案是:6.96,2.09×1024个。
(4)①、实验室要配制480mL溶液,只能选用500mL容量瓶,因此需要绿矾的质量为0.25×0.5×278=34.8 g;因此本题答案是:34.8。
②A 称量绿矾时,左码右物,称量物质量等于砝码质量-游码质量,称的绿矾质量偏小,实际浓度比所要求的偏小,可选;
B 使用容量瓶配制溶液时,俯视液面定容,造成溶液体积偏小,所得溶液的浓度偏高,不选;
C 没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中,造成溶质的量偏小,所得溶液的浓度偏低,可选;
D 容量瓶刚用蒸馏水洗净,没有干燥,不影响溶质的量和溶液的体积,所得溶液的浓度不变,不选;
E 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切,造成溶质的量减小,所得溶液的浓度偏低,可选;
F 把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用,相当于给溶液进行稀释,浓度偏小,可选;
综上所述,符合题意的选项有ACEF;本题答案是: ACEF。
③、定容时,若加蒸馏水时不慎超过刻度线,溶液体积无法确定,处理方法倒掉溶液,重新配制;综上所述,本题答案是:重新配制。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案