题目内容
1.在同一温度下,当弱电解质溶液a,强电解质溶液b,金属导体c的导电能力相同,若同时升高到相同温度,则它们的导电能力是( )| A. | a>b>c | B. | a=b=c | C. | c>a>b | D. | b>c>a |
分析 升高温度促进弱电解质电离,温度越高,金属晶体的电阻越大,据此分析解答.
解答 解:相同温度下,弱电解质溶液a、强电解质溶液b、金属导体c的导电能力相同,升高温度,促进弱电解质电离,导致弱电解质溶液中离子浓度大于强电解质溶液,所以导电能力a>b;
升高温度,金属晶体的电阻增大,则导电能力降低,所以三种物质导电能力大小顺序是a>b>c,故选A.
点评 本题考查物质导电能力大小判断,电解质溶液导电能力与离子浓度有关,金属导电能力与电阻有关,明确升高温度变化的物理量即可解答,题目难度不大.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
11.中草药陈皮中含有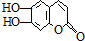 (碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
(碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
 (碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
(碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )| A. | 2moL,2moL | B. | 3 moL,3 moL | C. | 3 moL,4 moL | D. | 2 moL,4 moL |
12.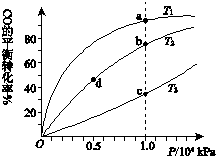 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )| A.温度: | T1>T2>T3 | |
| B.正反应速率: | υ(a)>υ(c) | υ(b)>υ(d) |
| C.平衡常数: | K(a)>K(c) | K(b)=K(d) |
| D.平均摩尔质量: | M(a)<M(c) | M(b)>M(d) |
| A. | A | B. | B | C. | C | D. | D |
16.下列实验获得成功的是( )
| A. | 欲证明放入硫酸溶液中的纤维素加热已发生水解可向所得溶液中加入银氨溶液,放在水浴中 | |
| B. | 欲证明蔗糖的水解产物有葡萄糖,可向试管中加入0.5g蔗糖及质量分数为10%的稀硫酸4mL,加热3~4分钟,再向试管中加入新制Cu(OH)2煮沸,观察有红色沉淀生成 | |
| C. | 为证明硬脂酸有酸性,可以向滴有酚酞的稀NaOH溶液加入硬脂酸,并加热 | |
| D. | 用灼烧的方法检验是羊毛线还是蚕丝线 |
6.下列叙述正确的是( )
| A. | 固体时能导电的晶体一定为金属晶体 | |
| B. | 某晶体固态不导电,水溶液能导电,该晶体一定为离子晶体 | |
| C. | 某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体 | |
| D. | 由原子构成的晶体均具有熔沸点高、硬度大的特性 |
13.下列除去杂质的实验方法正确的是( )
| A. | 除去铜器表面的铜绿[Cu2(OH)2CO3]:用硝酸浸泡,再用清水冲洗 | |
| B. | 除去K2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去KNO3晶体中少量NaCl:加水溶解、蒸发浓缩、冷却结晶、过滤洗涤 | |
| D. | 除去Mg(OH)2中少量的Ca(OH)2:加水,通入CO2 |
10.使2mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生最大程度的取代反应,则两个过程中消耗的氯气的总的物质的量是( )
| A. | 4mol | B. | 6mol | C. | 8mol | D. | 10mol |
11.有机化合物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项事实中,能说明上述观点的是( )
| A. | 甲醛和甲酸都能发生银镜反应 | |
| B. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| C. | 苯酚与溴水直接就可反应,而苯与溴反应则需要加铁屑 | |
| D. | 苯酚和乙酸都可以与氢氧化钠反应 |