��Ŀ����
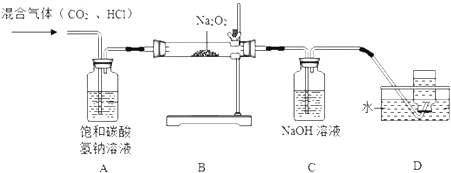
����Ŀ����ͼΪӲ֬��������ڼ���������ˮ���װ��ͼ������������Ӧʱ�IJ������£�

��1����Բ����ƿ��װ��7��8 gӲ֬���������Ȼ�����2��3 g�������ơ�5 mL ˮ��10 mL�ƾ�������ƾ���������________________________��
��2������ʯ��������Ӧ��������Լ10 min��������Ӧ������ɣ����õ��Ļ����Ϊ________(��������Һ����������Һ��������Һ������������)��
��3�������û�����м���________������һ��ʱ���Һ���Ϊ�������㣬������________�㣬���������Ϊ________��
��4��ͼ�г��������ܵ�����Ϊ________________________��
��5��д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________��
���𰸡� �ܽ�Ӳ֬������� ���� NaClϸ�� �� ���� �������������� 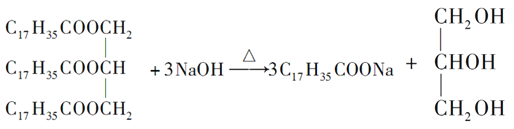
����������������Ҫ�ɷ��Ǹ�֬�����ƣ����ɶ���֬����ֲ������NaOH��Һ����������Ӧ��ȡ��������֬���л��������Ũ����Һ���ܻ��ܣ���Ҫ���������Ҵ���Ϊ�ܼ������Ͻ��裬�Լӿ�������Ӧ���ʡ���Ӧ��ɺ����ɸ�֬�����ơ����ͺ�ˮ�Ļ���Ϊ�˽���֬�����ƴӻ�����з����������Ҫ�����м��뱥��ʳ��ˮ(��ʳ��ϸ��)�Խ���֬�����Ƶ��ܽ�ȣ�ʹ��ӻ����������������Һ���ϣ�������̽�������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�