题目内容
【题目】下列说法中正确的是![]()
![]()
![]() 杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
![]() 同一周期从左到右,元素的第一电离能、电负性都是越来越大
同一周期从左到右,元素的第一电离能、电负性都是越来越大
![]() 分子中键能越大,表示分子拥有的能量越高
分子中键能越大,表示分子拥有的能量越高
![]() 所有的配合物都存在配位键
所有的配合物都存在配位键
![]() 所有含极性键的分子都是极性分子
所有含极性键的分子都是极性分子
![]() 熔融状态下能导电的化合物一定是离子化合物
熔融状态下能导电的化合物一定是离子化合物
![]() 所有的原子晶体都不导电
所有的原子晶体都不导电
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】D
【解析】①sp3杂化轨道是由同一个原子中能量最近的1个s轨道和3个p轨道混合起来形成的一组能量相同的新轨道;②同周期从左到右,元素的第一电离能呈增大趋势,第IIA族大于第IIIA族、第VA族大于第VIA族;③分子中键能越大,表明形成化学键时放出的能量越多,意味着化学键越稳定;④通常把金属离子(或原子)与某些分子或离子以配位键形成的化合物称为配合物;⑤含极性键的分子可能是极性分子如H2O、NH3等,也可能是非极性分子如CO2、CH4等;⑥熔融状态下能导电的化合物一定是离子化合物;⑦有的原子晶体能导电如锗等。
①只有同一原子中能量相近的不同类型的原子轨道才能杂化,sp3杂化轨道是由同一个原子中能量最近的1个s轨道和3个p轨道混合起来形成的一组能量相同的新轨道,①正确;②同周期从左到右,元素的第一电离能呈增大趋势,第IIA族大于第IIIA族、第VA族大于第VIA族,同周期从左到右电负性逐渐增大,②错误;③分子中键能越大,表明形成化学键时放出的能量越多,意味着化学键越稳定,③错误;④通常把金属离子(或原子)与某些分子或离子以配位键形成的化合物称为配合物,所有配合物中都存在配位键,④正确;⑤含极性键的分子可能是极性分子如H2O、NH3等,也可能是非极性分子如CO2、CH4等,⑤错误;⑥离子化合物中含阴、阳离子,共价化合物中含原子或分子,熔融状态下能导电的化合物一定是离子化合物,⑥正确;⑦有的原子晶体能导电如锗等,⑦错误;正确的有①④⑥,答案选D。

【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:____。
(2)c与a形成6个原子组成分子结构简式:__________,该分子是:_______(填“极性”或“非极性”)分子。
(3)表中O、P两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是__________________________;
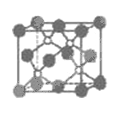
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
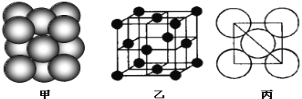
晶胞中i原子的配位数为___________,一个晶胞中i原子的数目为____________。