题目内容
25 ℃时,某溶液中由水电离出的H+的浓度为1×10-a mol/L,以下说法正确的是( )
| A.a>7时,水的电离一定受到促进 |
| B.a<7时,水的电离一定受到抑制 |
| C.a>7时,溶液的pH为a或14-a |
| D.a<7时,溶液的pH一定为a |
C
常温下水的离子积是1×10-14,由水电离出来的H+的浓度为1×10-7 mol/L,如果a>7肯定是水的电离受到了抑制,该溶液可能是酸溶液也可能是碱溶液。如果a<7,水的电离一定受到促进,是盐的水解起到了作用。A、B项正好答反,所以A、B都错。C选项,当a>7时,如果是碱溶液,则此时溶液中所有的H+都是由水电离产生的,此时溶液的pH=a,如果是酸溶液,则此时溶液中所有的OH-都是由水电离产生的,此时溶液的pOH=a,pH=14-a。D选项中,当a<7时,如果溶液呈酸性,溶液中的氢离子都是由水电离产生的,故有pH=a,如果溶液呈碱性,则溶液中所有的OH-都是由水电离产生的,得到pOH=a,pH=14-a。

练习册系列答案
相关题目
 M2+(aq)+2OH-(aq) Ksp=a。c(M2+)=b mol·L-1时,溶液的pH等于( )
M2+(aq)+2OH-(aq) Ksp=a。c(M2+)=b mol·L-1时,溶液的pH等于( )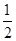 lg(
lg( )
)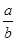 )
)


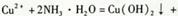
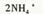
 H++OH-,在不同温度下其平衡常数为Kw(25 ℃)=1.0×10-14,Kw(35 ℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为Kw(25 ℃)=1.0×10-14,Kw(35 ℃)=2.1×10-14。则下列叙述正确的是