题目内容
6.A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.①D在周期表中的位置是第四周期第ⅠA族;
②用电子式表示A、B形成化合物的过程:
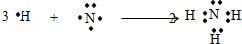 ;
;③D2C的电子式为
 .
.
分析 A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等,则A为H元素;B的原子半径是其所在主族中最小的,处于第二周期,B的最高价氧化物对应水化物的化学式为HBO3,最高正化合价为+5,处于ⅤA族,则B为N元素;C元素原子的最外层电子数比次外层少2个,则C应有三个电子层,最外层电子数为6,则C为S元素;C的阴离子与D的阳离子具有相同的电子排布,离子核外电子数为18,两元素可形成化合物D2C,D在第四周期第ⅠA族,则D为K,据此解答.
解答 解:A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等,则A为H元素;B的原子半径是其所在主族中最小的,处于第二周期,B的最高价氧化物对应水化物的化学式为HBO3,最高正化合价为+5,处于ⅤA族,则B为N元素;C元素原子的最外层电子数比次外层少2个,则C应有三个电子层,最外层电子数为6,则C为S元素;C的阴离子与D的阳离子具有相同的电子排布,离子核外电子数为18,两元素可形成化合物D2C,D在第四周期第ⅠA族,则D为K,
①由以上分析,B为K元素,位于元素周期表中第四周期第ⅠA族,故答案为:第四周期第ⅠA族;
②A、B形成的化合物为NH3,用电子式表示NH3的形成过程为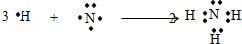 ,
,
故答案为: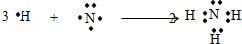 ;
;
③D2C为K2S,为离子化合物,含有离子键,其电子式为 ,故答案为:
,故答案为: .
.
点评 本题考查位置结构性质的相互关系应用,难度不大,注意正确推断元素所为解答该题的关键,注意掌握电子式的书写.

练习册系列答案
相关题目
17.如图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是( )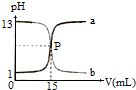

| A. | NaOH溶液的浓度为0.1 mol•L-1 | |
| B. | P点时恰好完全反应,溶液呈中性 | |
| C. | 曲线a是盐酸滴定氢氧化钠溶液的测定曲线 | |
| D. | 本实验的指示剂不能用甲基橙,只能用酚酞 |
11.下列用电子式表示物质的形成过程中正确的是( )
| A. | Na•+Cl:→[Na]+[•Cl:]- | B. | H2•+•O•→H:O:H | ||
| C. |  →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ | D. |  →H:F →H:F |
18.下列反应中反应物总能量高于生成物总能量的是( )
| A. | 碳酸钙受热分解 | B. | C和CO2 反应 | ||
| C. | Ba(OH)2晶体和氯化铵晶体反应 | D. | 氧化钙溶于水 |
15.除去下列物质中的杂质(括号内是杂质),能采用先与过量NaOH溶液充分反应再过滤的方法的是( )
| A. | Fe3O4(Al2O3) | B. | KCl(NaCl) | C. | SiO2(CaCO3) | D. | FeCl2溶液(FeCl3) |
16.根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
| A. | 第15列元素的最高价氧化物的化学式为R2O5 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | L层电子数为奇数的所有元素所在族的序数与元素原子L层电子数相等 | |
| D. | M层电子数为奇数的所有元素所在族的序数与元素原子M层电子数相等 |


 ;
; $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.