题目内容
17.如图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是( )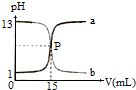
| A. | NaOH溶液的浓度为0.1 mol•L-1 | |
| B. | P点时恰好完全反应,溶液呈中性 | |
| C. | 曲线a是盐酸滴定氢氧化钠溶液的测定曲线 | |
| D. | 本实验的指示剂不能用甲基橙,只能用酚酞 |
分析 A、根据曲线b可以看出氢氧化钠溶液的pH=13,然后求出NaOH的物质的量浓度;
B、P点氢氧化钠与氯化氢恰好反应生成氯化钠;
C、根据曲线a的pH的变化趋势来判断;
D、氢氧化钠与盐酸恰好反应时溶液呈中性,可用酚酞或甲基橙做指示剂.
解答 解:A、根据曲线b可知NaOH溶液的pH=13,则氢氧化钠溶液的浓度为:(NaOH)=0.1mol/L,故A正确;
B、P点时氢氧化钠与盐酸恰好反应,溶液呈中性,故B正确;
C、曲线a的pH是由小到大,说明是氢氧化钠溶液滴定盐酸溶液的曲线,故C错误;
D、甲基橙的变色范围是3.1-4.4,酚酞的变色范围是8-10,且变色现象较明显,所以该中和滴定可以用酚酞或甲基橙作指示剂,故D错误;
故选AB.
点评 本题考查中和滴定、滴定曲线的分析应用,题目难度中等,试题借助于滴定曲线考查了中和滴定过程中PH的变化.,结合酸碱的性质分析解答,难点是酸碱指示剂的选取方法.

练习册系列答案
相关题目
8.下列过程属于氧化反应的是( )
| A. | 乙醇?乙醚 | B. | 乙醛?乙酸 | C. | 乙醛?乙醇 | D. | 乙酸?乙酸乙酯 |
5.下列叙述正确的是( )
| A. | L层电子数为奇数的所有元素都是非金属 | |
| B. | 只有第2列元素原子最外层有2个电子 | |
| C. | 第3、4、5、6周期元素的数目分别是8、18、32、32 | |
| D. | 元素周期表中第8、9、12列没有非金属 |
12.有机物种类繁多的主要原因是( )
| A. | 有机物都是天然产物 | |
| B. | 自然界中存在着多种形式的、大量的有机物 | |
| C. | 有机物除含碳元素外,还含有其他多种元素 | |
| D. | 碳原子能与其他原子形成四个共价键,且碳原子之间也能相互成键 |
2.关于下式表示的有机物的性质叙述中不正确的是( )


| A. | 它有酸性,能与纯碱溶液反应 | |
| B. | 它可以水解,水解产物只有一种 | |
| C. | 1 mol该有机物最多能和7 mol NaOH反应 | |
| D. | 该有机物能发生取代反应 |
9.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| C. | 乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O | |
| D. | 苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
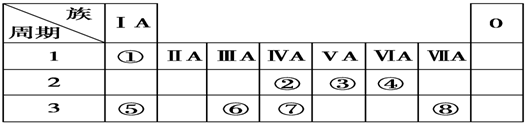
 .②的最高价氧化物的电子式是:
.②的最高价氧化物的电子式是:
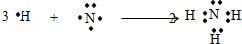 ;
; .
.