题目内容
【题目】在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成。请回答下列问题:
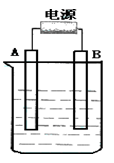
(1)B极板的名称是_____________,电解后溶液显_________(填“酸性”或“碱性”)写出电解时反应的总离子反应方程式为 ________________________
(2)若当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。要使电解后溶液恢复到电解前的状态,则需加入___________,其质量为__________g。(假设电解前后溶液的体积不变)
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是
方案 | A | B | 电解质溶液 |
A | 银 | 石墨 | AgNO3 |
B | 银 | 铁 | AgNO3 |
C | 铁 | 银 | Fe(NO3)3 |
D | 铁 | 银 | AgNO3 |
【答案】(1)阳极 酸性 2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
(2)CuO;2g(3)D
【解析】
试题分析:(1)电解池中有固体析出的电极是阴极,A电极表面有红色的固态物质生成,所以A极板的名称
是阴极,B极板的名称是阳极。溶液显蓝色,所以该溶液是硫酸铜溶液。电解时总离子方程式 2Cu2+ +2H2O![]() 2Cu +O2 ↑+ 4H+ 电解硫酸铜溶液生成硫酸,所以电解后溶液显酸性。(2)根据2Cu2++2H2O
2Cu +O2 ↑+ 4H+ 电解硫酸铜溶液生成硫酸,所以电解后溶液显酸性。(2)根据2Cu2++2H2O![]() 2Cu+O2↑+4H+知,阳极上生成氧气、阴极上生成铜,实质上相当于生成CuO,要使溶液恢复原状,应该加入CuO,根据Cu原子守恒得m(CuO)=
2Cu+O2↑+4H+知,阳极上生成氧气、阴极上生成铜,实质上相当于生成CuO,要使溶液恢复原状,应该加入CuO,根据Cu原子守恒得m(CuO)=![]() =2g,所以应加入CuO;质量2g.(3)电镀原理:铁是镀件做阴极,银是镀层金属做阳极,电解质溶液含镀层金属离子银离子。所以选D.
=2g,所以应加入CuO;质量2g.(3)电镀原理:铁是镀件做阴极,银是镀层金属做阳极,电解质溶液含镀层金属离子银离子。所以选D.

【题目】
(1)用托盘天平称取NaOH固体____________g。称量NaOH固体需注意:因NaOH具有腐蚀性,在称量时需用烧杯盛装NaOH固体;称量必须迅速,其原因是_________________________。
(2) 接下来完成此实验你将用到的仪器有玻璃棒、烧杯、_________________。
而某同学提出只需再选择带刻度的500 mL烧杯和玻璃棒,即可配制500 mL 0.10 mol/L的NaOH溶液;你对此方案的评价是_______________________。
(3) 若你从所配的溶液中取出50 mL于一试剂瓶中,请给它贴上标签,标签的内容是_________;
若再从中取出10 mL溶液加水稀释至20 mL,则此时溶液的物质的量浓度为____________。
(4) 下列操作对所配溶液浓度没有影响的是_______。
A.称量时已观察到NaOH表面潮湿 |
B.将烧杯中溶解后的溶液立即注入容量瓶,然后再添加蒸馏水至刻度线 |
C.摇匀定容后,又用胶头滴管向容量瓶中滴加蒸馏水至刻度线 |
D.配制溶液前用蒸馏水润洗容量瓶,但未烘干 |
【题目】除去下列物质中的杂质,所用试剂和方法不正确的是 ( )
物质 | 杂质 | 除杂所用试剂和方法 |
A.H2SO4 | HCl | AgNO3溶液、过滤 |
B.KNO3 | K2SO4 | Ba(NO3)2溶液、过滤 |
C.Cu | CuO | 盐酸、过滤 |
D.CaCO3 | CaO | H2O、过滤 |