题目内容
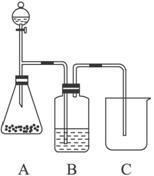
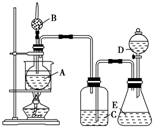
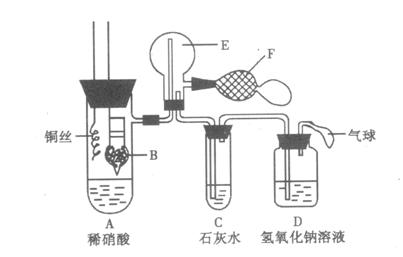
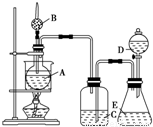
某学生设计如图实验装置用于制取纯净的无水氯化铜.根据各小题的要求,填写下列空白.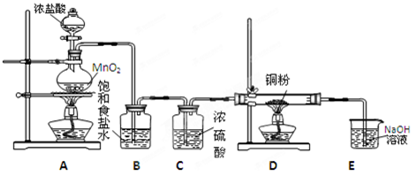
(1)装置B的作用是
(2)装置A中发生反应的化学方程式为
(3)装置E的作用是
分析:(1)根据实验室制取氯气的除杂方法思考,制备出的氯气中含有水蒸气和氯化氢需要除去;
(2)根据实验室制取氯气的反应原理和化学性质分析,实验室用二氧化锰和浓盐酸加热反应生成氯气,氯气和铜加热反应生成氯化铜;
(3)根据氯气的化学性质和尾气的处理方法解答,氯气有毒用氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
(2)根据实验室制取氯气的反应原理和化学性质分析,实验室用二氧化锰和浓盐酸加热反应生成氯气,氯气和铜加热反应生成氯化铜;
(3)根据氯气的化学性质和尾气的处理方法解答,氯气有毒用氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
解答:解:(1)制取氯气时需要加热,会使浓盐酸挥发出来,因此要用装置B除去HCl,可以使用饱和食盐水,即除去HCl又降低氯气在水中的溶解度;当氯气经过除杂装置B时,会使氯气中混入水蒸气,要用装置C中的浓硫酸吸收水蒸,
故答案为:除去Cl2中混有的HCl;除去Cl2中混有的水蒸气;
(2)实验室制取氯气,要用浓盐酸和二氧化锰反应,发生的是氧化还原反应,即化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;装置D中是纯净、干燥的氯气与铜反应生成氯化铜,即化学方程式为:Cu+Cl2
CuCl2,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;Cu+Cl2
CuCl2;
(3)在氯气与铜反应后,会有一部分氯气没有参与反应,直接排放带空气中会造成环境污染,因此要用氢氧化钠溶液(生成氯化钠和次氯酸钠)吸收氯气来防止污染空气,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:吸收多余的Cl2,防止污染空气;Cl2+2NaOH=NaCl+NaClO+H2O.
故答案为:除去Cl2中混有的HCl;除去Cl2中混有的水蒸气;
(2)实验室制取氯气,要用浓盐酸和二氧化锰反应,发生的是氧化还原反应,即化学方程式为:MnO2+4HCl(浓)
| ||
| ||
故答案为:MnO2+4HCl(浓)
| ||
| ||
(3)在氯气与铜反应后,会有一部分氯气没有参与反应,直接排放带空气中会造成环境污染,因此要用氢氧化钠溶液(生成氯化钠和次氯酸钠)吸收氯气来防止污染空气,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:吸收多余的Cl2,防止污染空气;Cl2+2NaOH=NaCl+NaClO+H2O.
点评:本题考查的是基本实验中的基本知识,要求学习气体制取时掌握制备原理,除杂方法,掌握基础是关键,题目难度中等.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
 某学生设计了如图所示的装置进行实验,各装置中所装试剂、实验操作及实验现象如下:
某学生设计了如图所示的装置进行实验,各装置中所装试剂、实验操作及实验现象如下: