题目内容
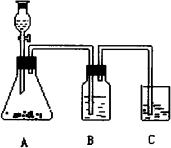
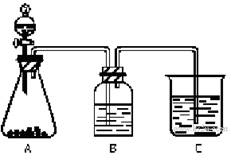
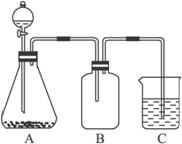
为了确认CH3COOH、H2CO3、H2SiO3的酸性强弱,某学生设计如图15-9所示装置,在不使用其他酸性溶液的条件下,能一次达到检验目的。 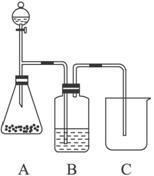
图15-9
(1)A装置中锥形瓶内装的某正盐固体是__________,分液漏斗中装的试剂是__________。
(2)B装置中所盛装的试剂是__________,该试剂的作用是_________________________。
(3)装置C中出现的现象是__________________________________________________。
(4)通过上述实验可证明三种酸的酸性强弱顺序为______________________________。
解析:首先弄懂复分解反应中酸A+盐B![]() 酸C+盐D的原理,若反应能进行,则A的酸性大于C。
酸C+盐D的原理,若反应能进行,则A的酸性大于C。
然后选择适当的试剂,如要检验CH3COOH酸性大于H2CO3,试剂为CH3COOH和Na2CO3。由于H2CO3不稳定,CO2的水溶液即为H2CO3,所以可以直接让生成的CO2通入到Na2SiO3水溶液中,但此时的CO2中含少量CH3COOH,所以在通入之前必须除杂。
答案:(1)碳酸钠 乙酸
(2)饱和NaHCO3溶液 除去CO2中的乙酸蒸气
(3)产生白色胶状沉淀
(4)CH3COOH>H2CO3>H2SiO3

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目