题目内容
某地质学家经勘测发现一种新的磁黄铁矿,主要成分为Fe1-xS1+x,杂质不含Fe、S.分析可知该磁黄铁矿中,铁元素中三价铁的质量分数为75%.取5吨73%的该磁黄铁矿,用接触法制硫酸,若沸腾炉中煅烧的损耗率为4%,接触室中反应的转化率为94%,SO3的吸收效率为97%,则最多可制得98.3%的浓硫酸的质量是 .(保留2位小数)
考点:化学方程式的有关计算
专题:计算题
分析:该磁黄铁矿中,铁元素中三价铁的质量分数为75%,则二价Fe的质量分数为25%,故三价铁与二价铁的物质的量之比为3:1,化学式Fe1-xS1+x可以改写为xFeS.Fe(1-x-x)S,则(1-x-x):x=3:1,解得x=0.2,故该磁黄铁矿为Fe0.8S1.2,根据质量分数计算的质量Fe0.8S1.2的质量,结合化学式计算S元素质量,再根据S~SO2~H2SO4计算,注意各步骤中涉及损耗率、转化率、吸收率都以S元素计算.
解答:
解:该磁黄铁矿中,铁元素中三价铁的质量分数为75%,则二价Fe的质量分数为25%,故三价铁与二价铁的物质的量之比为3:1,化学式Fe1-xS1+x可以改写为xFeS.Fe(1-x-x)S,则(1-x-x):x=3:1,解得x=0.2,故该磁黄铁矿为Fe0.8S1.2,5吨73%的该磁黄铁矿中Fe0.8S1.2的质量=5吨×73%=3.65吨,
令理论上最多可以生产98%的浓硫酸m吨,则:
S~~~~~~SO2~~~~~~H2SO4
32 98
3.65吨×
×(1-4%)×94%×97% m吨×98.3%
解得m=4.59,
故答案为:4.59吨.
令理论上最多可以生产98%的浓硫酸m吨,则:
S~~~~~~SO2~~~~~~H2SO4
32 98
3.65吨×
| 32×1.2 |
| 56×0.8+32×1.2 |
解得m=4.59,
故答案为:4.59吨.
点评:本题考查化学方程式有关计算,确定磁黄铁矿的化学式是关键,注意利用关系式进行解答,难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
能大量存在于同一溶液中,当改变条件使水电离出的时c(H+)=10-13mol?L-1,一定会发生反应的离子组是( )
| A、Fe2+、Na+、NO3-、Cl- |
| B、Ca2+、NH4+、SO42-、CO32- |
| C、Na+、Cu2+、Cl-、SO42- |
| D、Al3+、Na+、SO42-、HCO3- |
物质的性质决定着物质的用途,下列有关物质性质及其用途的说法,正确的是( )
| A、葡萄糖具有还原性,可用于医学尿糖的检验 |
| B、二氧化硫能使滴有酚酞的红色溶液褪色,说明其具有还原性 |
| C、酒精具有消毒杀菌作用,医用酒精的浓度越大,杀菌效果越好 |
| D、浓硫酸具有强氧化性,不能用于干燥硫化氢、碘化氢和二氧化硫等具有还原性的气体 |
0.2mol有机物和0.6mol O2在密闭容器燃烧后的产物为CO2和H2O,经过浓硫酸后,浓硫酸质量增加10.8g,再通过碱石灰被完全吸收,碱石灰质量增加17.6g,该有机物恰好与4.6g金属钠完全反应,则该有机物的结构简式为( )
| A、CH3CH2OH |
| B、CH3CHO |
| C、CH3CH2CH2OH |
| D、CH3COOH |

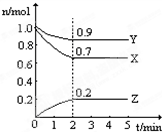 某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: