题目内容
11.有关如图所示化合物的说法不正确的是( )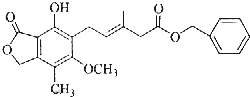
| A. | 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 | |
| B. | 1mol该化合物最多可以与4molNaOH反应 | |
| C. | 既可以催化加氢,又可以使酸性KMnO4溶液褪色 | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
分析 A.该有机物分子中含有碳碳双键和甲基,能够溴发生加成反应,也能够与氯气发生取代反应;
B.该有机物分子中含有2个酯基、1个酚羟基,1mol该有机物最多消耗3mol氢氧化钠;
C.苯环和碳碳双键能够催化加氢,碳碳双键、苯环上的甲基、酚羟基能够被酸性高锰酸钾溶液氧化;
D.该有机物分子中不含有羧基,不能与碳酸氢钠反应.
解答 解:A.该有机物分子中含有官能团碳碳双键,可以与Br2的CCl4溶液发生加成反应,该有机物分子中还含有甲基,还可以在光照下与Br2发生取代反应,故A正确;
B.2个-COOC-及1个酚-OH均能与碱反应,则1mol该化合物最多可以与3molNaOH反应,故B错误;
C.其分子中含有C=C,则既可以催化加氢,又可以使酸性KMnO4溶液褪色,故C正确;
D.该有机物含酚-OH,能与FeCl3溶液发生显色反应,但酸性较弱,不能与与NaHCO3溶液反应,故D错误;
故选BD.
点评 本题考查有机物的结构与性质,题目难度中等,明确烯烃、苯酚的性质是解答本题的关键,注意熟练掌握常见有机物结构与性质.

练习册系列答案
相关题目
1.在一定温度下,可逆反应A(气)+3B(气)?2C(气)达到平衡的标志是( )
| A. | 2v正(A)=v正(C) | |
| B. | 单位时间内生成n摩A,同时生成3n摩B | |
| C. | A、B、C的浓度不再变化 | |
| D. | A、B、C的分子数之比为1:3:2 |
2.下列混合物,不论它们以何种比例混合,只要总质量一定,经完全燃烧后产生二氧化碳和水的量也一定的是( )
| A. | 乙炔和乙苯 | B. | 甲烷和乙烷 | ||
| C. | 乙醛和丙酮 | D. | 乙酸和乳酸[CH3CH(OH)COOH] |
16.下列叙述错误的是( )
| A. | 阴、阳离子通过静电吸引所形成的化学键,叫离子键 | |
| B. | 活泼金属元素与活泼非金属元素化合时,形成的是离子键 | |
| C. | 某元素最外层只有一个电子,它与卤素原子结合时所形成的化学键不一定是离子键 | |
| D. | 全部由非金属元素组成的化合物可能是离子化合物 |
3.下列化合物中阴阳离子半径之和最大的离子化合物是( )
| A. | NaF | B. | NaCl | C. | SO2 | D. | CaCl2 |
20.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 锂(Li)与水反应比钠与水反应剧烈 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | Mg(OH)2的碱性比Al(OH)3的碱性强 |
1.工业上以铝土矿(主要成分是Al2O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
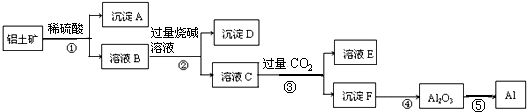
下列叙述错误的是( )

下列叙述错误的是( )
| A. | 沉淀A主要是SiO2 | B. | 步骤②的目的是分离Fe3+和Al3+ | ||
| C. | 溶液E溶质主要有碳酸钠和硫酸钠 | D. | ⑤主要是把电能转化为化学能 |
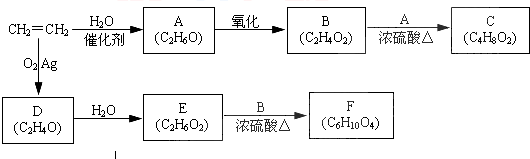
 ,在催化剂存在条件下1molD与2molH2反应可以生成乙;丙中含有两个-CH3
,在催化剂存在条件下1molD与2molH2反应可以生成乙;丙中含有两个-CH3
 .
. .
.
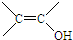 、
、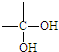 结构非常不稳定,会迅速转变为
结构非常不稳定,会迅速转变为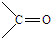
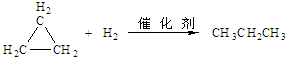
 .
.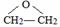 .
. .
.