题目内容
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,脱氧的同时可降低温度,延长糕点保质期 |
| B.脱氧过程中铁做原电池正极,电极反应为:Fe—2e— = Fe2+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e— = 4OH— |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
D
解析试题分析:A.铁粉、氯化钠溶液、炭粉构成原电池,原电池放电过程是放热反应,故A错误;B.脱氧过程中铁作原电池负极,负极上铁失电子生成亚铁离子,电极反应为:Fe-2e-→Fe2+,错误;C.脱氧过程中碳做原电池正极,故C错误;D.原电池的正极反应式为2H2O + O2 + 4e— = 4OH—,由电子守恒可知消耗氧气为0.01mol,后发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3,消耗氧气0.005mol,总共消耗氧气为0. 015mol,在标准状况下的体积为336m L.D对。
考点:原电池原理、正负极的判断、电极反应式的书写。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
寒冷的冬天,经常使用暖宝宝,暖宝宝中装的是铁粉、活性炭、无机盐等物质,打开包装以后,可以连续12个小时释放热量,以下分析错误的是
| A.将化学能转化为热能 |
| B.其发热原理与钢铁的吸氧腐蚀相同 |
| C.铁作负极,电极反应为:Fe – 3e → Fe3+ |
| D.活性炭作正极,电极反应为:2H2O + O2 + 4e → 4OH- |
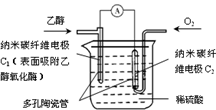
来自法国格勒诺布尔(Grenoble)约瑟夫·傅立叶大学的研究小组发明了第一块可为人体人造器官提供电能的可植入的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生的总反应为C6H12O6+6O2=6CO2+6H2O(酸性环境),下列对该电池说法不正确的是
| A.该生物燃料电池不可以在高温下工作 |
| B.电池的负极反应为:C6H12O6+6H2O-24e-=6CO2+24H+ |
| C.消耗1mol氧气则转移4mole-,H+会向负极移动 |
| D.今后的研究方向是怎样提高葡萄糖生物燃料电池的效率,从而在将来达到可以利用葡萄糖生物燃料电池为任何可植入医疗设备提供电能 |
用惰性电极电解某金属元素R的硝酸盐R(NO3)n溶液,通电一段时间后,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的相对原子质量为M,设NA为阿伏加德罗常数的值,下列叙述中不正确的是
A.电路中通过电子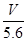 NA NA | B.n = 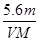 |
C.溶液中H+增加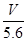 NA NA | D.n = 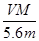 |
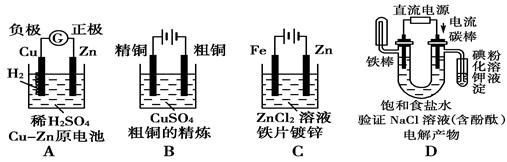
不能用Fe+H2SO4=FeSO4+H2↑表示的是( )
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |