题目内容
【题目】某中学学习小组模拟工业烟气脱硫(SO2)。
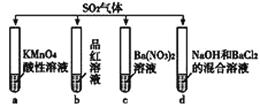
(1)甲组采用如下装置脱硫(部分装置略)。

① CaO脱硫后的产物是_________。
② b中品红很快褪色,说明脱硫效果不好。下列措施能提高脱硫效果的是_____。
ⅰ. 加快SO2气体流速
ⅱ. 将堆集在一起的CaO平铺在整个玻璃管
ⅲ. 加热a,脱硫效果可能会更好
③ 小组拟通过CaO的增重评价其脱硫能力。需要测量的数据是_______。
(2)乙组选用AgNO3溶液脱除SO2 。

现象:通入SO2,立即生成大量白色沉淀A。
对白色沉淀A的成分进行探究,提出假设:
假设1:发生了氧化还原反应,依据是AgNO3溶液中含有O2、![]() 等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。
等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。
假设2:发生了复分解反应,依据是SO2与水生成酸,能与AgNO3溶液发生复分解反应。
实验探究:
① 取沉淀A,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,无明显变化。
② 取______,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,产生沉淀。
实验证明“假设1”不成立。
③ 为进一步确认“假设2”,向A中加入浓HNO3,立即产生红棕色气体。加入浓硝酸的目的是________;经确认,反应后混合液存在SO![]() 。
。
实验证明“假设2”成立。
④ 产生沉淀A的化学方程式是_________。AgNO3溶液具有良好的脱硫能力,但因其价格高,未能大规模使用。
(3)丙组用NaClO脱除SO2,用1 L 0.1 mol/L 的NaClO溶液最多可以吸收标准状况下的SO2_______L。
【答案】 CaSO3 ⅱ、ⅲ 装置a的质量;盛放CaO后装置a的质量;吸收SO2后装置a的质量 Ag2SO4固体 检验白色沉淀是否具有还原性 H2O + SO2 = H2SO3 , H2SO3 + 2AgNO3 = Ag2SO3↓+ 2HNO3 2.24
【解析】(1)①二氧化硫是酸性氧化物,氧化钙是碱性氧化物,二者反应生成亚硫酸钙,因此CaO脱硫后的产物是CaSO3。②ⅰ. 加快SO2气体流速不利于二氧化硫吸收,错误;ⅱ. 将堆集在一起的CaO平铺在整个玻璃管,增大反应物接触面积,有利于能提高脱硫效果,正确;ⅲ. 加热a加快反应速率,脱硫效果可能会更好,正确,答案选ⅱ、ⅲ;③要通过CaO的增重评价其脱硫能力,需要知道反应前后固体增加的质量,因此需要测量的数据是装置a的质量、盛放CaO后装置a的质量、吸收SO2后装置a的质量。(2)②要证明“假设1”不成立,需要证明沉淀A不是硫酸银,因此需要做对比实验,即取Ag2SO4固体,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,产生沉淀,这说明“假设1”不成立。③浓HNO3具有强氧化性,所以加入浓硝酸的目的是检验白色沉淀是否具有还原性;④根据复分解反应原理可知产生沉淀A的化学方程式是H2O+SO2=H2SO3、H2SO3+2AgNO3=Ag2SO3↓+2HNO3。(3)1 L 0.1 mol/L的NaClO溶液中次氯酸钠的物质的量是0.1mol,次氯酸钠的还原产物是氯化钠,因此可以得到0.2mol电子,二氧化硫的氧化产物是硫酸,所以根据电子得失守恒可知最多可以吸收SO20.1mol,在标准状况下的体积是2.24L。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案