题目内容
【题目】
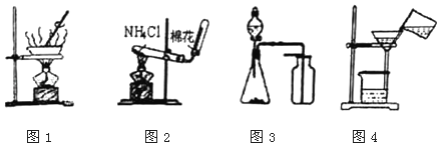
A. 用托盘天平直接称量烧碱4.0g
B. 在蒸发皿中灼烧CuSO4·5H2O晶体以除去结晶水
C. 用标准盐酸溶液滴定未知浓度的氨水,用酚酞作指示剂
D. 配制0.9%的氯化钠溶液时,将称量的氯化钠放入烧杯中加计量的水搅拌溶解
【答案】D
【解析】试题分析:A、烧碱具有腐蚀性且易吸水,所以称量氢氧化钠固体应该放在烧杯中,A不正确;B、固体加热应该放在坩埚中,B不正确;C、盐酸与氨水恰好反应时溶液显酸性,应该用甲基橙作指示剂,C不正确;D、配制一定物质的量浓度溶液时固体溶解或稀释应该在烧杯中,冷却后再转移至容量瓶,D正确,答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)的分解反应。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15 | 20 | 25 | 30 | 35 |
平衡总压强/kPa | 5.7 | 8.3 | 12 | 17.1 | 24 |
平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
①该可逆反应的平衡常数的表达式为________________________
②可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中CO2的体积分数不变
D.密闭容器中总压强不变
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25 ℃下达到分解平衡。若在恒温下增大容器体积,氨基甲酸铵固体的质量将________(填“增加”、“减少”或“不变”)。该反应的焓变ΔH______0(填“>”、“=”或“<”,下同),熵变ΔS_______0
(2)在高温下一氧化碳可将二氧化硫还原为单质硫。
已知:①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②CO2(g)+C(s)===2CO(g) ΔH2=+172.5 kJ·mol-1
③S(s)+O2(g)===SO2(g) ΔH3=-296.0 kJ·mol-1
请写出CO与SO2反应的热化学方程式_________________________________________________________