题目内容
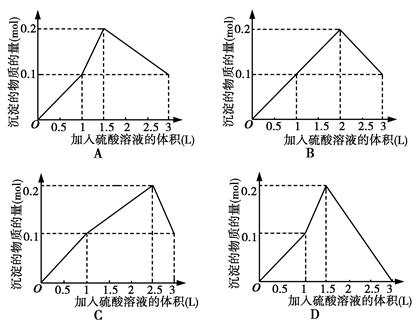
在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol·L-1H2SO4溶液,下列图像中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是( )

点拨:本题考查离子反应过程中图像的分析,考查考生对混合溶液中离子反应过程实质的理A
解。难度中等。
解。难度中等。
混合溶液中加入H2SO4,首先发生Ba(OH)2+H2SO4===BaSO4↓+2H2O,0.1 mol H2SO4刚好与0.1 mol Ba(OH)2完全反应生成0.1 mol BaSO4沉淀,且H2SO4电离出的H+与Ba(OH)2电离出的OH-也刚好完全中和,再加入H2SO4,则发生反应:AlO2—+H++H2O===Al(OH)3↓,即加入0.5 mol H2SO4时生成Al(OH)3为0.1 mol,继续加入H2SO4,则Al(OH)3会溶解,最终只有BaSO4沉淀。

练习册系列答案
相关题目
 HCO3—+OH-
HCO3—+OH-
 )+c(OH-)
)+c(OH-)