题目内容
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。该电池工作时的总反应为:NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法正确的是
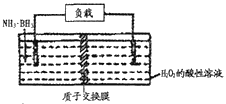
A. 正极附近溶液的pH减小
B. 电池工作时,H+通过质子交换膜向负极移动
C. 消耗3.1g氨硼烷,理论上通过内电路的电子为0.6ml
D. 负极电极反应为:NH3·BH3+2H2O-6e-= NH4++BO2-+6H+
【答案】D
【解析】H2O2为正极得到电子发生还原反应,电极反应式为3H2O2+6H++6e-═6H2O ,正极消耗氢离子,正极附近溶液的pH增大,故A错误;放电时,阳离子向正极移动,H+通过质子交换膜向正极移动,故B错误;负极电极反应式为NH3BH3+2H2O-6e-=NH4BO2+6H+,则消耗3.lg即0.1mol氨硼烷,理论上通过外电路的电子为0.6ml,故C错误; 根据电池工作时的总反应为:NH3BH3+3H2O2═NH4BO2+4H2O可知,左侧NH3BH3为负极失电子发生氧化反应,电极反应式为NH3·BH3+2H2O-6e-=NH4++BO2-+6H+,故D正确。

练习册系列答案
相关题目
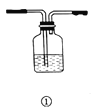
【题目】下列有关实验操作的主要仪器、注意事项及应用举例都正确的是( )

![]()
选项 | 实验操作 | 主要仪器 | 注意事项 | 应用举例 |
A | 洗气 | ① | 从长管进气,短管出气 | 用饱和碳酸氢钠溶液除去CO2气体中的SO2气体 |
B | 气体干燥 | ② | 从粗管进气,细管出气 | 用无水氯化钙作干燥剂干燥氨气 |
C | 分液 | ③ | 先将下层液体从下口放出,再将上层液体从下口放出 | 分离植物油和水的混合物 |
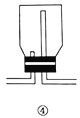
D | 气体收集 | ④ | 从长管进气,短管出气 | 收集氯气 |
A. A B. B C. C D. D