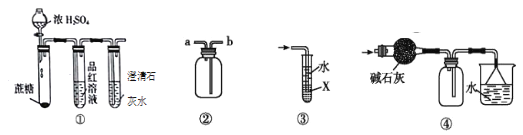
题目内容
【题目】回答下列问题:
(1)碳原子的核外电子排布式为____________。与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是_________________。
(2)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:________。

(3)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
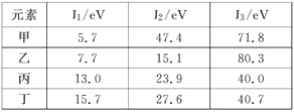
下列说法正确的是________(填字母)。
A.甲的金属性比乙强 B.乙的化合价为+1价
C.丙不可能为非金属元素 D.丁一定为金属元素
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
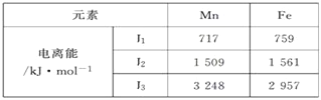
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价电子排布式:________,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_________________________。
【答案】 1s22s22p2 N原子的2p轨道达到半充满结构,比较稳定 1s22s22p63s2 A 3d5 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少
【解析】(1)碳原子的核外电子排布式为:1s22s22p2;N原子的核外电子排布式为:1s22s22p3,O原子核外电子排布式为1s22s22p4,2p轨道半充满的原子能量低,较稳定,所以与碳同周期的非金属元素N的第一电离能大于O的第一电离能;(2)从表中电离能数值来看,A、B的第三电离能出现突跃,可见它们是第ⅡA族元素,因A、B均为短周期元素,且B的第一、二电离能均比A的小,故B是镁。镁原子的电子排布式为:1s22s22p63s2;(3)甲、乙、丙、丁为第三周期元素,甲元素的第一电离能远远小于第二电离能,说明A元素最外层有1个电子,失去1个电子时达到稳定结构,所以甲为Na元素;乙元素的第二电离能远远小于第三电离能,则乙元素最外层有2个电子,失去两个电子后达到稳定结构,所以乙为Mg元素;丙、丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层大于3个电子,丙、丁一定为非金属元素。A.甲为Na元素,乙为Mg元素,故甲的金属性比乙强,选项A正确;B.乙为Mg元素,化合价为+2价,选项B错误;C、丙、丁一定为非金属元素,选项C错误;D、丙、丁一定为非金属元素,选项D错误。答案选A;(4)Mn的原子序数为25,失去2个电子变为Mn2+,则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),故其价电子排布式为:3d5;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少,故气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难。

【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是( )
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
A.A
B.B
C.C
D.D