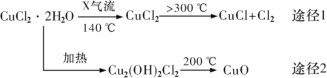题目内容
【题目】已知4NH3(g)+5O2 (g)=4NO(g) + 6H2O (g) ,若化学反应速率分别用v (NH3)、v (O2 )、v(NO)、v (H2O)[单位:mol/ ( L s)] 表示,则正确的关系是
A.![]() v(NH3)=v (O2)B.
v(NH3)=v (O2)B.![]() v (O2) =v(H2O)
v (O2) =v(H2O)
C.v(NH3)=![]() v(H2O)D.v(O2) =
v(H2O)D.v(O2) =![]() v(NO)
v(NO)
【答案】BD
【解析】
同一化学反应中,不同物质表示的化学反应速率之比等于对应化学计量数之比,据此计算判断。
A.v(NH3):v(O2)=4:5,则![]() v(NH3)=v(O2),A错误;
v(NH3)=v(O2),A错误;
B.v(O2):v(H2O)=5:6,则![]() v(O2)=v(H2O),B正确;
v(O2)=v(H2O),B正确;
C.v(NH3):v(H2O)=4:6=2:3,则v(NH3)=![]() v(H2O),C错误;
v(H2O),C错误;
D.v(O2):v(NO)=5:4,则v(O2)=![]() v(NO),D正确。
v(NO),D正确。
答案选BD。

 阅读快车系列答案
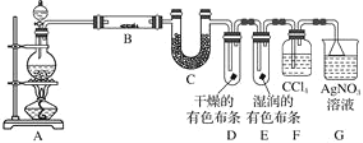
阅读快车系列答案【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
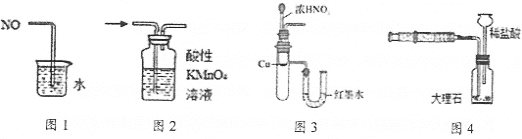
A.图1可用于吸收多余的NO
B.图2可用于检验SO2的漂白性
C.图3可用于说明铜与浓硝酸反应的能量变化
D.图4可用于测定CO2的生成速率
【题目】25 ℃时,0.1 mol·L-1HA溶液中 =108,0.01 mol·L-1BOH溶液pH=12。请回答下列问题:
=108,0.01 mol·L-1BOH溶液pH=12。请回答下列问题:
(1)HA的电离常数Ka为________,BOH是________(填“强电解质”或“弱电解质”)。
(2)pH相等的BOH溶液与BA溶液,分别加热到相同的温度后BOH溶液的pH________(填“>”“=”或“<”)BA溶液的pH。
(3)已知碳酸的Ka1=4.3×10-7,Ka2=5.6×10-11,向等浓度的Na2CO3和NaA的溶液中滴加盐酸直至过量,则与H+作用的粒子依次为___________________。
(4)25 ℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________。
②0.10 mol·L-1 NaHSO3溶液中离子浓度由大到小的顺序为_____________________。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为______________________。